题目内容
【题目】秋冬季是雾霾高发的季节,其中汽车尾气和燃煤尾气是造成雾霾的主要原因之一。
(1)工业上利用甲烷催化还原NO,可减少氮氧化物的排放。
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ·mol1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ·mol1
甲烷直接将NO2还原为N2的热化学方程式为_____________________________________。
(2)汽车尾气催化净化是控制汽车尾气排放、减少汽车尾气污染的最有效的手段,主要原理为2NO(g)+2CO(g)![]() N2(g)+2CO2(g)ΔH<0
N2(g)+2CO2(g)ΔH<0
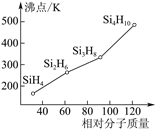
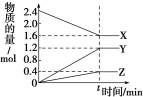
T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,保持温度和体积不变,反应过程(0~15min)中NO的物质的量随时间变化如上图所示。
①已知:平衡时气体的分压=气体的体积分数×体系的总压强,T℃时达到平衡,此时体系的总压强为p=20MPa,则T℃时该反应的压力平衡常数Kp=_______;平衡后,若保持温度不变,再向容器中充入NO和CO2各0.3mol,平衡将_____(填“向左”、“向右”或“不”)移动。
②15min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是__(填序号)
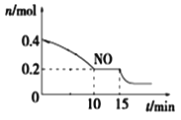
A.增大CO浓度B.升温C.减小容器体积D.加入催化剂
(3)工业上常采用“碱溶液吸收”的方法来同时吸收SO2,和氮的氧化物气体(NOx),如用氢氧化钠溶液吸收可得到Na2SO3、NaHSO3、NaNO2、NaNO3等溶液。已知:常温下,HNO2的电离常数为Ka=7×10-4,H2SO3的电离常数为Ka1=1.2×10-2、Ka2=5.8×10-8。
①常温下,相同浓度的Na2SO3、NaNO2溶液中pH较大的是______溶液。
②常温下,NaHSO3显___性(填“酸”“碱”或“中”,判断的理由是(通过计算说明)_____________。
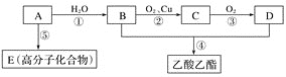
(4)铈元素(Ce)是镧系金属中自然丰度最高的一种,常见有+3、+4两种价态。雾霾中含有大量的污染物NO,可以被含Ce4+的溶液吸收,生成NO2-、NO3-(二者物质的量之比为1∶1)。可采用电解法将上述吸收液中的NO2-转化为无毒物质,同时再生Ce4+,其原理如图所示。
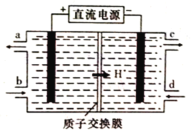
①Ce4+从电解槽的_____(填字母代号)口流出。
②写出阴极的电极反应式:_______________________________。
【答案】CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH=-867kJ·mol1 0.0875(MPa)-1或![]() (MPa)-1 不 AC Na2SO3 酸 因为HSO3-的电离常数Ka2=5.8×10-8,水解常数Kh=
(MPa)-1 不 AC Na2SO3 酸 因为HSO3-的电离常数Ka2=5.8×10-8,水解常数Kh=![]() ≈8.3×10-13,电离常数大于水解常数,所以溶液显酸性 a 2NO2-+8H++6e=N2↑+4H2O
≈8.3×10-13,电离常数大于水解常数,所以溶液显酸性 a 2NO2-+8H++6e=N2↑+4H2O
【解析】
(4)电解过程中Ce3+在阳极失电子,变为Ce4+,则b进Ce3+,a出Ce4+,NO2-在阴极得电子变为N2,则d进NO2-,c出N2。
(1)①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574kJ·mol1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160kJ·mol1
![]() 得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH=
得:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH=![]() =-867kJ·mol1,故答案为:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH=-867kJ·mol1;
=-867kJ·mol1,故答案为:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH=-867kJ·mol1;
(2)①由图可知,NO起始物质的量为0.4mol,0到15min共减少了0.2mol,则 ,平衡时p(NO)= 20MPa×
,平衡时p(NO)= 20MPa×![]() =
=![]() MPa,同理可得:p(CO)=
MPa,同理可得:p(CO)=![]() MPa,p(N2)=
MPa,p(N2)=![]() MPa,p(CO2) =
MPa,p(CO2) =![]() MPa,所以Kp=
MPa,所以Kp=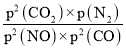 =
=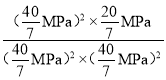 =0.0875(MPa)-1或
=0.0875(MPa)-1或![]() (MPa)-1。再向容器中充入NO和CO2各0.3mol,加入的NO和CO2物质的量相等,那么二者引起压强增大量相等,假设二者引起的压强增量分别为p,则Qc=
(MPa)-1。再向容器中充入NO和CO2各0.3mol,加入的NO和CO2物质的量相等,那么二者引起压强增大量相等,假设二者引起的压强增量分别为p,则Qc=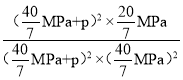 =
=![]() (MPa)-1,Qc=Kp,平衡不移动,故答案为:0.0875(MPa)-1或
(MPa)-1,Qc=Kp,平衡不移动,故答案为:0.0875(MPa)-1或![]() (MPa)-1;不;
(MPa)-1;不;
②由图可知NO物质的量减小,说明平衡正向移动。
A.增大CO浓度,平衡正向移动,NO物质的量减小,A正确;
B.升温,平衡逆向移动,NO物质的量增大,B错误;
C.减小容器体积,等同于增大压强,平衡正向移动,NO物质的量减小,C正确;
D.加入催化剂,反应速率增大,但平衡不移动,NO物质的量不变,D错误;
故答案为:AC;
(3)①HNO2的电离常数为Ka=7×10-4,H2SO3的电离常数为Ka1=1.2×10-2、Ka2=5.8×10-8可知,HNO2的酸性强于HSO3-的酸性,则NO2-的水解程度小于SO32-,所以相同浓度的Na2SO3、NaNO2溶液,Na2SO3的碱性更强,pH更大,故答案为:Na2SO3;
②HSO3-+H2O![]() H2SO3,Ka2×Kh=Kw,故HSO3-的水解常数Kh=
H2SO3,Ka2×Kh=Kw,故HSO3-的水解常数Kh=![]() ≈8.3×10-13,又因为HSO3-的电离常数Ka2=5.8×10-8,所以,HSO3-的电离常数大于水解常数,常温下,NaHSO3显酸性,故答案为:酸;因为HSO3-的电离常数Ka2=5.8×10-8,水解常数Kh=
≈8.3×10-13,又因为HSO3-的电离常数Ka2=5.8×10-8,所以,HSO3-的电离常数大于水解常数,常温下,NaHSO3显酸性,故答案为:酸;因为HSO3-的电离常数Ka2=5.8×10-8,水解常数Kh=![]() ≈8.3×10-13,电离常数大于水解常数,所以溶液显酸性;
≈8.3×10-13,电离常数大于水解常数,所以溶液显酸性;
(4)①生成Ce4+,则Ce3+-e-= Ce4+,Ce4+在阳极生成,从a口流出,故答案为:a;
②NO2-转化为无毒物质,则NO2-在阴极得电子,转化为N2,结合电子得失守恒、电荷守恒可得阴极电极反应为:2NO2-+8H++6e=N2↑+4H2O,故答案为:2NO2-+8H++6e=N2↑+4H2O。

 阅读快车系列答案
阅读快车系列答案【题目】某化学小组以下列4种物质的溶液作为研究对象,比较不同物质的羟基中氢原子的活泼性。①乙酸 ②苯酚 ③碳酸 ④乙醇
I.甲同学设计并实施了如下实验方案。
编号 | 实验操作 | 实验现象 | 结论及解释 |
1 | 分别取4种溶液,滴加紫色石蕊溶液 | 溶液变红的是①③溶液 | 略 |
2 | 将CO2通入C6H5ONa溶液中 | 方程式:______________。 | |
3 | 配制等物质的量浓度的CH3COONa、 NaHCO3溶液,并比较其pH | NaHCO3溶液pH大于 CH3COONa溶液 | 略 |
4 | 向含酚酞的NaOH溶液中,各滴加等量的②④两种溶液 | ④中无明显现象 ②中红色明显变浅 | 滴加②时方程式:______。 |
结论:4种物质的羟基中的氢原子的活泼性由强到弱的顺序是(填序号)______________。 | |||
II.乙同学对甲同学的实验提出如下改进方案,能一次比较乙酸、碳酸和苯酚的羟基中氢原子的活泼性,实验仪器如下图所示。

(1)利用上述仪器组装实验装置,其中A管插入(填字母,下同)D中,B管插入__________中,C管插入_________中。
(2)丙同学查资料发现乙酸有挥发性,于是在试管F之前增加了一个盛有________溶液的洗气装置,使乙同学的实验设计更加完善。