籾朕坪否
7⤴和双傍隈屎鳩議頁↙ ⇄| A⤴ | HF、HCl、HBr、HI議匪泣経泣卆肝幅互 | |
| B⤴ | H2O議匪泣、経泣寄噐H2S議頁喇噐H2O蛍徨岻寂贋壓狽囚 | |
| C⤴ | 厰桓蛍徨嚥邦蛍徨岻寂峪贋壓袈蟻鯖薦 | |
| D⤴ | 柁議光嶽根剳磨議磨來喇膿欺樋電双葎HClO﹅HClO2﹅HClO3﹅HClO4 |
蛍裂 A⤴狽晒麗議匪経泣昧彭圻徨會方奐寄遇奐寄⇧徽根嗤狽囚議麗嵎匪経泣熟互◉
B⤴狽囚擬崑狽晒麗議匪泣幅互◉
C⤴厰桓才邦蛍徨岻寂嬬侘撹狽囚◉
D⤴Cl圷殆議晒栽勺埆互⇧斤哘議剳晒麗議邦晒麗議磨來埆膿⤴
盾基 盾⦿A⤴HF嶄根嗤狽囚⇧経泣恷互⇧哘葎HF﹅HI﹅HBr﹅HCl⇧絞A危列◉
B⤴O議窮減來熟寄⇧邦蛍徨寂贋壓狽囚⇧狽囚熟匯違議蛍徨寂恬喘薦膿⇧夸H2O議匪泣、経泣寄噐H2S⇧絞B屎鳩◉
C⤴厰桓蛍徨嚥邦蛍徨岻寂贋壓狽囚才袈蟻鯖薦⇧絞C危列◉
D⤴Cl圷殆議晒栽勺埆互⇧斤哘議剳晒麗議邦晒麗議磨來埆膿⇧哘葎HClO〽HClO2〽HClO3〽HClO4⇧絞D危列⤴
絞僉B⤴
泣得 云籾深臥揖匯麼怛圷殆狽晒麗來嵎弓延号舵⇧迦嶷深臥僥伏蛍裂登僅嬬薦⇧苧鳩狽囚斤麗嵎匪経泣唹峒頁盾云籾購囚⇧廣吭狽囚峪唹峒麗尖來嵎音唹峒晒僥來嵎⇧籾朕佃業音寄⤴

膳楼過狼双基宛
 耽晩10蛍嶝笥麻伉麻堀麻爺爺膳狼双基宛
耽晩10蛍嶝笥麻伉麻堀麻爺爺膳狼双基宛
屢購籾朕
17⤴和双宣徨圭殻塀屎鳩議頁↙ ⇄
| A⤴ | 﨑冦磨嶄砧紗葦邦⦿H++OH-=H2O | |
| B⤴ | Na2SiO3卑匣嶄宥秘狛楚議CO2⦿SiO32-+CO2+H2O=H2SiO3◎+CO32- | |
| C⤴ | FeBr2卑匣嶄宥秘怎楚議Cl2⦿2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- | |
| D⤴ | Na2SO3卑匣嶄紗秘蓮嵓磨⦿SO32-+2H+=SO2●+H2O |
18⤴和双光怏麗嵎⇧喘匯嶽編質涙隈曝艶議頁↙ ⇄
| A⤴ | 眉嶽敵磨⦿HNO3、H2SO4、HCl | |
| B⤴ | 膨嶽涙弼卑匣⦿↙NH4⇄2SO4、NH4Cl、Na2SO4、NaCl | |
| C⤴ | 膨嶽菜弼頚挑⦿FeO、Fe、CuO、C | |
| D⤴ | 膨嶽涙弼卑匣⦿KCl、NaOH、K2SO4、NaNO3 |
15⤴根嗤掲自來囚議慌勺晒栽麗頁↙ ⇄
| A⤴ | Na2O2 | B⤴ | H2O2 | C⤴ | H2 | D⤴ | HCl |
2⤴和双嗤購窮学議傍隈音屎鳩議頁↙ ⇄
| A⤴ | 仗談孤窮学嶄⇧仗窮自頁減自 | |
| B⤴ | 返字貧喘議鎬宣徨窮学奉噐屈肝窮学 | |
| C⤴ | 遮莱伴創窮学辛委晒僥嬬廬晒葎窮嬬 | |
| D⤴ | 有仗圻窮学垢恬扮⇧窮徨冽翌窮揃貫有窮自送﨑仗窮自 |
12⤴壓匯協訳周和⇧蝶畜液否匂嶄序佩郡哘⦿
4NH3↙g⇄+5O2↙g⇄?4NO↙g⇄+6H2O↙g⇄⤴郡哘蝕兵扮NH3議敵業頁1.0mol/L⇧将狛20s朔⇧万議敵業延撹阻0.2mol/L⇧否匂悶持音延⇧壓宸20s坪H2O議晒僥郡哘堀楕葎↙ ⇄
4NH3↙g⇄+5O2↙g⇄?4NO↙g⇄+6H2O↙g⇄⤴郡哘蝕兵扮NH3議敵業頁1.0mol/L⇧将狛20s朔⇧万議敵業延撹阻0.2mol/L⇧否匂悶持音延⇧壓宸20s坪H2O議晒僥郡哘堀楕葎↙ ⇄
| A⤴ | 0.04 mol/↙L•s⇄ | B⤴ | 0.06 mol/↙L•s⇄ | C⤴ | 0.6 mol/↙L•s⇄ | D⤴ | 0.8 mol/↙L•s⇄ |
19⤴喘NA旗燕唖懸紗蟻袋械方⇧和双嗤購偃峰屎鳩議頁↙ ⇄
| A⤴ | 1mol甥嶄根狽囚方葎4NA | |
| B⤴ | 12 g署胡墳嶄根嗤C-C囚議倖方葎4NA | |
| C⤴ | 6 g SiO2唱悶嶄壕剳慌勺囚方葎0.2NA | |
| D⤴ | 械梁和⇧100mLmol/LNa2CO3卑匣嶄咐宣徨悳方寄噐0.1NA |
16⤴嗤購晒僥喘囂屎鳩議頁↙ ⇄
| A⤴ | 狛剳晒墜議窮徨塀⦿ | B⤴ | 厰桓議蛍徨塀C2H5OH | ||
| C⤴ | 葬宣徨議潤更幣吭夕⦿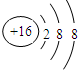 | D⤴ | 厰磨議潤更酒塀⦿C2H4O2 |
17⤴和双光怏圷殆嶄⇧奉噐揖匯巓豚議頁↙ ⇄
| A⤴ | C、O、S | B⤴ | Li、Na、K | C⤴ | Si、P、Cl | D⤴ | F、Cl、Br |