题目内容
13.下列说法正确的是( )| A. | 光导纤维、合成纤维和人造纤维都是有机高分子化合物 | |
| B. | 合金拓展了金属材料的使用范围,合金中也可能含有非金属元素 | |
| C. | H2O2是一种绿色氧化剂,可氧化酸性高锰酸钾而产生O2 | |
| D. | 对“地沟油”进行分馏可以制得汽油、煤油,达到变废为宝的目的 |
分析 A、相对分子质量在10000以上的有机化合物为高分子化合物;
B、合金中可能含有非金属元素;
C、高锰酸钾的氧化性比过氧化氢的氧化性强;
D、地沟油的主要成分为油脂,油脂为高级脂肪酸甘油酯;据此解答即可.
解答 解:A、光导纤维的成分是二氧化硅,不是高分子化合物,故A错误;
B、合金是由两种或两种以上的金属与金属(或非金属)经一定方法所合成的具有金属特性的物质.合金材料中一定有金属,也可能含有非金属元素,故B正确;
C、高锰酸钾的氧化性比过氧化氢强,与高锰酸钾溶液反应应是过氧化氢被氧化生成水,故C错误;
D、地沟油的主要成分为油脂,油脂为高级脂肪酸甘油酯,分馏是物理变化,不可能得到汽油、煤油,故D错误,故选B.
点评 本题考查较为综合,涉及高分子化合物概念、油脂的性质、氧化还原氧化剂氧化性强弱判断等知识,为高频考点,侧重于学生的分析能力和基础知识的综合理解和运用的考查,难度不大,注意相关知识的积累.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
1.分子式为C3H6Cl2的有机物,若再有一个氢原子被氯原子取代,生成的C3H5Cl3有两种同分异构体,原有的C3H6Cl2应该是( )
| A. | 1,3-二氯丙烷 | B. | 1,1-二氯丙烷 | C. | 1,2-二氯丙烷 | D. | 2,2-二氯丙烷 |
8.在密闭体积不变的真空容器中加入一定量纯净的氨基甲酸铵固体,(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g),已知25℃时,平衡气体总浓度为2.4×10-3mol•L-1,下列说法中正确的是( )
| A. | 密闭容器中气体的平均相对分子质量不变则该反应达到平衡状态 | |
| B. | 20℃时,氨基甲酸铵的分解平衡常数为2.048×10-9mol3•L-3 | |
| C. | 恒温下压缩体积,NH3的体积分数不变 | |
| D. | 再加入一定量氨基甲酸铵,可加快正反应反应速率 |
18.能源是人类生存与发展必不可缺的物质,对传统能源进行脱硫、脱硝处理,提高新能源在能源消费中的比倒是改变目前我国频发的雾霾天气的有效措施.
(1)肼(N2H4)和化合物甲是一种重要的火箭推进剂,甲分子与肼分子具有相同的电子数,二者反应的生成物中有l0e-分子,另一种生成物为极稳定的单质,写出该反应的化学方程式N2H4+2H2O2=N2↑+4H2O;
(2)对燃煤产生的尾气进行回收处理,有助于空气质量的改善,还能变废为宝,尾气处理过程中涉及到的主要反应如下:
①2CO(g)+SO2(g)=S(g)+2CO2(g)△H=+8.0kJ•mol-1
②2H2 (g)+SO2(g)=S(g)+2H2O(g)△H=+90.4kJ•mol-1
③2CO(g)+O2(g)=2CO2 (g)△H=-566.0kJ•mol-1l
④2H2 (g)+O2 (g)=2H2O(g)△H=-483.6kJ•mol-1
S(g)与O2(g)反应生成SO2 (g)的热化学方程式为S(g)+O2(g)=SO2 (g)△H=-574kJ•mol-1.
(3)煤碳液化也有助于减少雾霾天气的发生,液化反应之一为:
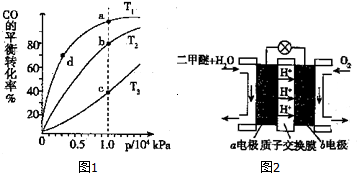
CO(g)+2H2(g)?CH3OH(g)△H<O;按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图1所示,则正反应速率:v(a)、v(b)、v(c)、v(d)由小到大的顺序为v(d)<v(a)<v(b)<v(c);
实际生产条件控制在T1℃、1×l04kPa左右,选择此压强的理由是压强为1×l04kPa左右,CO的转化率已经很大,压强再增大,CO转化率提高不大,生成成本增大,得不偿失.
(4)工业上生产新能源二甲醚(CH3OCH3)的原理之一为:
2CO2(g)+6H2( g)?CH3OCH3(g)+3H2O(g).相同温度下,在两个容器中进行上述反应,某时刻两容器中各气态物质的浓度(mol•L1-)及正逆反应速率之间的关系如下表所示:
填写表中空白处并写出其推测过程I处于平衡状态,则平衡常数k=$\frac{1×1{0}^{-4}×(1×1{0}^{-4})^{3}}{(1×1{0}^{-2})^{2}×(1×1{0}^{-2})^{6}}$=1,Ⅱ中浓度商Qc=$\frac{1×1{0}^{-4}×(2×1{0}^{-4})^{3}}{(2×1{0}^{-2})^{2}×(1×1{0}^{-2})^{6}}$=2,则Qc>K=1,故反应向逆反应方向进行.
(5)二甲醚(燃烧热为1455kJ/mol)燃料电池是一种绿色电池,其工作原理如图2所示,a、b均为惰性电极,a极的电极反应式为CH3OCH3-12e-+3H2O═2CO2↑+12H+;当消耗1molO2时,通过质子交换膜的质子数为4NA;
若电池工作时消耗1mol二甲醚所能产生的最大电能为1320kJ,则该燃料电池的工作效率为90.7% (燃料电池的工作效率是指电池所产生的最大电能与燃料燃烧时所能释放的全部热能之比).

(1)肼(N2H4)和化合物甲是一种重要的火箭推进剂,甲分子与肼分子具有相同的电子数,二者反应的生成物中有l0e-分子,另一种生成物为极稳定的单质,写出该反应的化学方程式N2H4+2H2O2=N2↑+4H2O;
(2)对燃煤产生的尾气进行回收处理,有助于空气质量的改善,还能变废为宝,尾气处理过程中涉及到的主要反应如下:
①2CO(g)+SO2(g)=S(g)+2CO2(g)△H=+8.0kJ•mol-1
②2H2 (g)+SO2(g)=S(g)+2H2O(g)△H=+90.4kJ•mol-1
③2CO(g)+O2(g)=2CO2 (g)△H=-566.0kJ•mol-1l
④2H2 (g)+O2 (g)=2H2O(g)△H=-483.6kJ•mol-1
S(g)与O2(g)反应生成SO2 (g)的热化学方程式为S(g)+O2(g)=SO2 (g)△H=-574kJ•mol-1.
(3)煤碳液化也有助于减少雾霾天气的发生,液化反应之一为:
CO(g)+2H2(g)?CH3OH(g)△H<O;按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图1所示,则正反应速率:v(a)、v(b)、v(c)、v(d)由小到大的顺序为v(d)<v(a)<v(b)<v(c);
实际生产条件控制在T1℃、1×l04kPa左右,选择此压强的理由是压强为1×l04kPa左右,CO的转化率已经很大,压强再增大,CO转化率提高不大,生成成本增大,得不偿失.
(4)工业上生产新能源二甲醚(CH3OCH3)的原理之一为:
2CO2(g)+6H2( g)?CH3OCH3(g)+3H2O(g).相同温度下,在两个容器中进行上述反应,某时刻两容器中各气态物质的浓度(mol•L1-)及正逆反应速率之间的关系如下表所示:
| 容器 | c(CO2) | c(H2) | c(CH3OCH3) | c(H2O) | v(正)和v(逆)大小比较 |
| I | 1.0×10-2 | 1.0×10-2 | 1.0×10-4 | 1.0×10-4 | v(正)=v(逆) |
| Ⅱ | 2.0×10-2 | 1.0×10-2 | 1.0×10-4 | 2.0×10-4 | v 正)< v(逆)(填>、<、=) |
(5)二甲醚(燃烧热为1455kJ/mol)燃料电池是一种绿色电池,其工作原理如图2所示,a、b均为惰性电极,a极的电极反应式为CH3OCH3-12e-+3H2O═2CO2↑+12H+;当消耗1molO2时,通过质子交换膜的质子数为4NA;
若电池工作时消耗1mol二甲醚所能产生的最大电能为1320kJ,则该燃料电池的工作效率为90.7% (燃料电池的工作效率是指电池所产生的最大电能与燃料燃烧时所能释放的全部热能之比).
5.燃烧某混合气体,所产生的CO2的质量一定大于燃烧相同质量丙烯所产生的CO2的质量,该混合气体是( )
| A. | 丙烷、丁烯 | B. | 乙炔、丙烷 | C. | 乙烷、乙烯 | D. | 乙炔、乙烯 |
2.下列有关物质结构的表述正确的是( )
| A. | 次氯酸的电子式  | B. | 氯化钠的分子式 NaCl | ||
| C. | 硫原子的最外层电子排布式3s23p4 | D. | 钠离子的结构示意图 |
3.下列有关实验事实中,能说明侧链对苯环性质有影响的是( )
| A. | 苯酚能和NaOH溶液反应 | |
| B. | 甲苯与液溴,铁作催化剂的反应 | |
| C. | 甲苯能被酸性高锰酸钾氧化 | |
| D. | 1mol邻二甲苯与3mol H2发生加成反应 |
 .
.
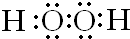 ,C元素在周期表中的位置是第二周期、第ⅦA族.
,C元素在周期表中的位置是第二周期、第ⅦA族.