题目内容
【题目】我国农业因遭受酸雨而造成的损失每年高达15亿多元,为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。
(1)现有雨水样品1份,每隔一段时间测定该雨水样品的pH所得数据如下:
测试时间/h | 0 | 1 | 2 | 3 | 4 |
雨水的pH | 4.75 | 4.62 | 4.56 | 4.55 | 4.54 |
分析数据,回答以下问题:
①雨水样品呈酸性的原因是________________________________(用化学方程式表示)。
②如果将刚取样的上述雨水和自来水(含有氯气)混合,pH将________(填“变大”“变小”或“不变”)。
(2)测定雨水样品时,每隔一定时间测定一次pH,发现pH逐渐变小,其原因可能是_______(用化学方程式表示)。
(3)举一例说明这种雨水将给环境中的生物或非生物造成的影响________________。
【答案】SO2+H2O![]() H2SO3 变小 2H2SO3+O2==2H2SO4 酸雨可腐蚀金属、建筑物,破坏植物,污染湖泊导致大量鱼类及水生生物死亡(任选1例,其它合理答案均可)
H2SO3 变小 2H2SO3+O2==2H2SO4 酸雨可腐蚀金属、建筑物,破坏植物,污染湖泊导致大量鱼类及水生生物死亡(任选1例,其它合理答案均可)
【解析】
正常雨水中,CO2+H2O![]() H2CO3,由于碳酸显酸性,所以正常雨水显酸性,且pH大约为5.6。当雨水中溶入一定量SO2后,SO2与水反应生成亚硫酸,从而使雨水的酸性增强,pH减小。当pH<5.6,雨水这就成为酸雨。在酸雨中,H2SO3易被空气中的氧气氧化为硫酸,导致酸性增强,pH减小。
H2CO3,由于碳酸显酸性,所以正常雨水显酸性,且pH大约为5.6。当雨水中溶入一定量SO2后,SO2与水反应生成亚硫酸,从而使雨水的酸性增强,pH减小。当pH<5.6,雨水这就成为酸雨。在酸雨中,H2SO3易被空气中的氧气氧化为硫酸,导致酸性增强,pH减小。
(1)①雨水样品呈酸性,主要是SO2溶于水并与水反应,原因是SO2+H2O![]() H2SO3。答案为:SO2+H2O
H2SO3。答案为:SO2+H2O![]() H2SO3;
H2SO3;
②如果将刚取样的上述雨水和自来水(含有氯气)混合,则会发生反应H2SO3+Cl2+H2O==H2SO4+2HCl,pH将变小。答案为:变小;
(2)测定雨水样品时,每隔一定时间测定一次pH,发现pH逐渐变小,主要是H2SO3被空气中O2氧化所致,其原因可能是2H2SO3+O2==2H2SO4。答案为:2H2SO3+O2==2H2SO4;
(3)举一例说明这种雨水将给环境中的生物或非生物造成的影响酸雨可腐蚀金属、建筑物,破坏植物,污染湖泊导致大量鱼类及水生生物死亡(任选1例,其它合理答案均可)。答案为:酸雨可腐蚀金属、建筑物,破坏植物,污染湖泊导致大量鱼类及水生生物死亡(任选1例,其它合理答案均可)。

【题目】钒及其化合物在工业上有许多用途。某钒精矿的主要成分及质量分数如下表:
物质 | V2O5 | V2O3 | K2O | SiO2 | Fe2O3 | Al2O3 |
质量分数% | 0.81 | 1.70 | 2.11 | 63.91 | 5.86 | 12.51 |
一种从该钒精矿中提取五氧化二钒的流程如下:
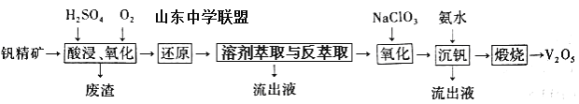
回答下列问题:
(1)“酸浸、氧化”时,V2O3转化为VO2+,反应的离子方程式为____________________________________;若用浓盐酸代替硫酸,V2O5转化为VO2+,同时生成有毒的黄绿色气体,反应的化学方程式为__________________。
(2)萃取剂对四价钒具有高选择性,且萃取Fe3+而不萃取Fe2+,所以萃取前可用____________(填名称,下同)对浸出液进行“还原”处理。为检验“还原”后的滤液中是否含有Fe3+,可选用的化学试剂是____________________。
(3)“溶剂萃取与反萃取”可表示为:VO2+ + (HR2PO4)2(O)![]() VO(R2PO4)2(O)+ 2H+。其中(HR2PO4)2(O)为萃取剂,为了提高VO2+的产率,反萃取剂应该呈 __________性(填“酸”“碱”或“中”)。
VO(R2PO4)2(O)+ 2H+。其中(HR2PO4)2(O)为萃取剂,为了提高VO2+的产率,反萃取剂应该呈 __________性(填“酸”“碱”或“中”)。
(4)“氧化”中,欲使3molVO2+变为VO2+,则需要氧化剂NaClO3至少为____________mol。
(5)单质钒可用于制造特种合金钢。以五氧化二钒和金属钙为原料在高温条件下可制备单质钒,表示制备过程的化学方程式为________________________________________。