题目内容
4.下列说法不正确的是( )| A. | 碳化硅可作砂纸、砂轮的磨料 | |
| B. | 地沟油没有利用价值,可用燃烧法处理 | |
| C. | 食盐、食醋、纯碱、小苏打是常见的厨房用品 | |
| D. | 开发和利用太阳能是节约化石能源,弥补能源不足的途径 |
分析 A、碳化硅是原子晶体,硬度较大;
B、地沟油属于酯类,可以再利用;
C、食盐、食醋、纯碱、小苏打均在生活中有重要应用;
D、太阳能是取之不尽用之不竭的.
解答 解:A、碳化硅是原子晶体,硬度较大,可做砂纸、砂轮的磨料,故A正确;
B、地沟油属于酯类,可以用于制肥皂、生物柴油等实现再利用,而燃烧可以引起空气污染,故B错误;
C、食盐和食醋是重要的调味品,纯碱、小苏打可用于食品的发酵等,故C正确;
D、太阳能是取之不尽用之不竭的,且对环境无污染,故D正确.
故选B.
点评 本题考查了生活中的化学知识,难度不大,注重化学知识的积累.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
13.下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1mol•L-1某二元弱酸酸式盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A) | |
| B. | 25℃,pH=12的氨水和pH=2的盐酸溶液等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| C. | 将pH=5的醋酸溶液稀释后,恢复至原温度,pH和Kw均增大 | |
| D. | 向NH4HSO4溶液中加入等物质的量的NaOH形成的溶液中:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
14.下列变化过程中,一定发生了化学变化的是( )
| A. | 蒸馏 | B. | 升华 | C. | 爆炸 | D. | 燃烧 |
12.下列有关说法中错误的是( )
| A. | 用NaOH溶液滴定醋酸时,可用酚酞试液作指示剂 | |
| B. | 花生油、菜子油漕油等水解时可得到一种共同的产物 | |
| C. | NH3+HCl=NH4Cl能自发进行,其△H一定小于零 | |
| D. | 甲烷和氯气反应与苯和硝酸反应的反应类型不同 |
19.下列说法正确的是( )
| A. | 碘元素遇淀粉溶液均变蓝色 | |
| B. | 质子数为86、中子数为51的氡原子可表示为:$\stackrel{137}{86}$Rn | |
| C. | CS2的电子式::$\underset{\stackrel{..}{S}}{..}$:$\underset{\stackrel{..}{C}}{..}$:$\underset{\stackrel{..}{S}}{..}$: | |
| D. | 6.0g醋酸晶体中含有H+的数目为0.1NA |
9.下列说法正确的是( )
| A. | 漂白液中添加醋酸可提高漂白速率 | |
| B. | 石油裂化是为了除去石油中的杂质 | |
| C. | 淀粉溶液可鉴别加碘盐的真伪 | |
| D. | 蛋白质、淀粉、纤维素都能在人体内水解并提供能量 |
16.X、Y、Z、W、R属于短周期元素.已知它们都不是稀有气体元素,X的原子半径最大,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数m-n,W元素与Z元素同主族,R元素原子与Y元素原子的核外电子数之比为2:1. 下列叙述错误的是( )
| A. | X与Y形成的两种化合物中阴、阳离子的个数比均为1:2 | |
| B. | Y分别与Z、W、R以两种元素组成的常见化合物有5种 | |
| C. | Z、W、R最高价氧化物对应水化物的酸性强弱顺序是:R>W>Z | |
| D. | Y的氢化物比R的氢化物稳定,Y的氢化物熔沸点比R的氢化物低 |
13.某pH=1的X溶液中可能含有Fe2+、Al3+,NH4+、CO32-、SO42-、Cl-中的若干种,现取X溶液进行连续实验,实验过程及产物如下:下列说法正确的是( )
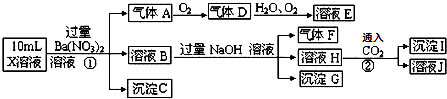

| A. | 气体A是NO2 | |
| B. | X中肯定存在Fe2+、A13+、NH4+、SO42- | |
| C. | 溶液E和气体F不能发生化学反应 | |
| D. | X中不能确定的离子是 A13+和C1- |
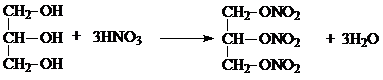 .
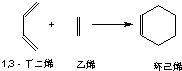
.
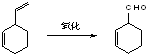
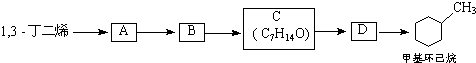
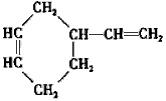 ;B
;B