题目内容
15.如图 是环己烷的结构简式,下列说法不正确的是( )
是环己烷的结构简式,下列说法不正确的是( )| A. | 环己烷不属于烃 | |
| B. | 环己烷的分子式为C6H12 | |
| C. | 环己烷是苯和氢气加成产物 | |
| D. | 1 mol环己烷完全燃烧消耗氧气的物质的量为9 mol |
分析 A、只有C、H两种元素组成的化合物是烃;
B、依据环己烷的结构简式判断分子式即可;
C、苯与氢气加成反应生成环己烷;
D、依据烃的燃烧通式进行计算即可.
解答 解:A、 只含有C、H两种元素,属于烃,故A错误;
只含有C、H两种元素,属于烃,故A错误;
B、饱和烷烃通式为:CnH2n+2,由于一个环为1个不饱和度,故环己烷的分子式为C6H12,故B正确;
C、苯在Ni作催化剂条件下,1mol苯分子与3mol氢气加成生成环己烷,故C正确;
D、烃完全燃烧生成二氧化碳和水,C6H12+9O2$\stackrel{点燃}{→}$6CO2+6H2O,故D正确,故选A.
点评 本题主要考查的是环己烷的结构、分子式确定、燃烧通式以及苯的加成反应等,难度不大.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
6.下表是周期表中的一部分,根据A-N在周期表中的位置,按要求回答下列问题:
(1)表中元素,氧化性最强的单质是F2,还原性最强的单质是Na(用相关的元素符号或分子式表示)
(2)最高价氧化物的水化物酸性最强的是高氯酸,呈两性的是氢氧化铝.(本小题均填物质的名称)
(3)在B、C、D、F、G、H中,原子半径从大到小的顺序为的是Na>Mg>Al>C>N>F.(用元素符号表示).
(4)在D、F、M的离子半径从大到小的顺序为的是Cl->F->Na+.(用离子符号表示).
(5)F的最高价氧化物对应的水化物和H的最高价氧化物对应的水化物反应的离子方程式是Al(OH)3+OH-═AlO2-+2H2O.
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | J | K | M | N |
(2)最高价氧化物的水化物酸性最强的是高氯酸,呈两性的是氢氧化铝.(本小题均填物质的名称)
(3)在B、C、D、F、G、H中,原子半径从大到小的顺序为的是Na>Mg>Al>C>N>F.(用元素符号表示).
(4)在D、F、M的离子半径从大到小的顺序为的是Cl->F->Na+.(用离子符号表示).
(5)F的最高价氧化物对应的水化物和H的最高价氧化物对应的水化物反应的离子方程式是Al(OH)3+OH-═AlO2-+2H2O.
3.烷烃分子可以看作由以下基团组合而成:-CH3、-CH2-、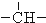 、
、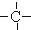 .如某烷烃分子中同时存在这四种基团,-CH2-、
.如某烷烃分子中同时存在这四种基团,-CH2-、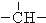 、
、 分别为m、n、a个,则该烷烃中-CH3的数目应是( )
分别为m、n、a个,则该烷烃中-CH3的数目应是( )
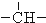 、
、 .如某烷烃分子中同时存在这四种基团,-CH2-、
.如某烷烃分子中同时存在这四种基团,-CH2-、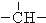 、
、 分别为m、n、a个,则该烷烃中-CH3的数目应是( )
分别为m、n、a个,则该烷烃中-CH3的数目应是( )| A. | 2m+3n+4a | B. | m+2n+2a | C. | n+2a+2 | D. | m+n+2a |
10.下列叙述不正确的是( )
| A. | 原子核外每层最多容纳的电子数为2n2个(n为电子层) | |
| B. | 同一原子核外的M层上的电子数一定比L层上的电子数多 | |
| C. | 如果原子只有一个电子层,该原子的质子数不超过2个 | |
| D. | 1~18号元素,每层电子数都满足2n2个电子的元素只有2种 |
20.下列比较中不正确的是( )
| A. | 离子半径:Cl->F->Na+ | B. | 热稳定性:HCl>H2S>HF | ||
| C. | 酸性:HClO4>H2SO4>H2CO3 | D. | 熔点:金刚石>晶体硅>CO2 |
7.化学与能源开发、环境保护、生产生活等密切相关.下列有关说法正确的是( )
| A. | 二氧化硫可用于纸浆漂白,表明二氧化硫具有还原性 | |
| B. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| C. | 为防止月饼等富脂食品氧化变质,常在包装袋中放入生石灰 | |
| D. | Na2O2可用作呼吸面具的供氧剂 |
4.下列有关实验的操作与现象描述及相关结论正确的是( )
| A. | 向无水乙醇中加入浓H2SO4,加热至170°C产生的气体通入酸性KMnO4溶液,红色褪去,证明生成的气体全部是乙烯 | |
| B. | 润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复2~3次 | |
| C. | 某些强氧化剂如氯酸钾、硝酸钾等或其混合物不能研磨,否则可能引起爆炸 | |
| D. | 取5mL0.1mol•L-1KI溶液,滴加0.1mol•L-1FeCl3溶液5~6滴,继续加入2mLCCl4,充分振荡后静置,取上层溶液加KSCN溶液,无明显现象 |
5.HF气体分子间容易缔合.某HF气体由HF、(HF)2、(HF)3三者混合而成,其平均相对分子质量为42,则(HF)3的体积分数可能为( )
| A. | 51% | B. | 56% | C. | 49% | D. | 10% |
