题目内容
9.下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成反应是( )| A. | NH4HCO3═NH3↑+CO2↑+H2O | B. | NH3+HCl=NH4Cl | ||
| C. | 2KOH+Cl2=KCl+KClO+H2O | D. | 2K2O2+2CO2=2K2CO3+O2 |
分析 根据活泼金属和活泼非金属之间易形成离子键,同种非金属元素之间易形成非极性共价键,不同种非金属元素之间易形成极性共价键,化学反应的实质是旧化学键的断裂和新化学键的形成,据此分析解答.
解答 解:A.NH3、CO2、H2O中只含有极性共价键,则生成物中只有极性共价键的形成,故A错误;
B.NH4Cl中含有离子键和极性共价键,则生成物中只有极性共价键、离子键的断裂,故B错误;
C.KOH中含有离子键和极性共价键,Cl2中含有非极性共价键,则反应物中有离子键、非极性共价键断裂和极性键的断裂,而生成物中无非极性共价键的形成,故C错误;
D.K2O2为含有非极性键的离子化合物,CO2中含有极性键,则反应物中离子键、极性共价键和非极性共价键断裂,故D正确;
故选:D.
点评 本题以化学反应与化学键的关系,难度不大,明确物质中存在化学键的类型是解答本题的关键,注意非金属元素之间易形成共价键,但铵盐除外,铵盐中含有离子键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.下列粒子(分子或离子)均含有18个电子:
请回答下列问题:
(1)A的元素符号是K,B2-的结构示意图是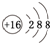 .
.
(2)C与D混合,发生反应的化学方程式为F2+2HCl═2HF+Cl2.
(3)E的电子式是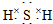 ;F的水溶液常用于消毒剂,F的化学式是H2O2.
;F的水溶液常用于消毒剂,F的化学式是H2O2.
| 粒子 | A+ | B2- | C | D | E | F |
| 组成特点 | 单核离子 | 化合物, 双核分子 | 单质, 双核分子 | 化合物, 三核分子 | 化合物, 四核分子 | |
(1)A的元素符号是K,B2-的结构示意图是
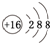 .
.(2)C与D混合,发生反应的化学方程式为F2+2HCl═2HF+Cl2.
(3)E的电子式是
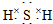 ;F的水溶液常用于消毒剂,F的化学式是H2O2.
;F的水溶液常用于消毒剂,F的化学式是H2O2.
20.如表为元素周期表中的一部分,列出10种元素在周期表中的位置.用化学符号回答下列各题.
(1)10种元素中,化学性质最不活泼的是Ar.
(2)②③④三种元素形成的离子中,离子半径由大到小的顺序是K+>Ca2+>Mg2+.
(3)①③⑤三种元素最高价氧化物对应的水化物中,碱性最强的是NaOH.
(4)元素⑦的氢化物的化学式为H2O;该氢化物常温下和②单质反应的化学方程式是2K+2H2O=2KOH+H2↑;若该氢化物和元素⑧的单质反应,则化学方程式为Cl2+H2O=HCl+HClO.
(5)⑨的最高价氧化物对应水化物的化学式为HBrO4;①和⑨两元素形成化合物为NaBr;该化合物灼烧时火焰颜色为黄色;该化合物的溶液与元素⑧的单质反应的离子方程式为2Br-+Cl2═2Cl-+Br2.
(6)①和⑤元素最高价氧化物对应水化物相互反应的离子方程式为Al(OH)3+OH-═AlO2-+2H2O.
族 周期 | ||||||||
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)②③④三种元素形成的离子中,离子半径由大到小的顺序是K+>Ca2+>Mg2+.
(3)①③⑤三种元素最高价氧化物对应的水化物中,碱性最强的是NaOH.
(4)元素⑦的氢化物的化学式为H2O;该氢化物常温下和②单质反应的化学方程式是2K+2H2O=2KOH+H2↑;若该氢化物和元素⑧的单质反应,则化学方程式为Cl2+H2O=HCl+HClO.
(5)⑨的最高价氧化物对应水化物的化学式为HBrO4;①和⑨两元素形成化合物为NaBr;该化合物灼烧时火焰颜色为黄色;该化合物的溶液与元素⑧的单质反应的离子方程式为2Br-+Cl2═2Cl-+Br2.
(6)①和⑤元素最高价氧化物对应水化物相互反应的离子方程式为Al(OH)3+OH-═AlO2-+2H2O.
4.同主族元素形成的同一类化合物往往在结构和性质上很相似.化合物PH4I是一种白色晶体,则对PH4I的叙述不正确的是( )
| A. | 它可由PH3和HI化合而成 | |
| B. | 加热时PH4I可以分解,而且有颜色变化 | |
| C. | 它可以跟NaOH反应 | |
| D. | 它是一种共价化合物 |
14.常温下,下列表述正确的是( )
| A. | pH=13的NaOH溶液中含有H+的浓度为0.l mol/L | |
| B. | 向NaHCO3溶液中加入少量NaOH固体,可抑制HCO3-的水解,使c(HCO3-)增大 | |
| C. | 将任意量的CH3COOH溶液与NaOH溶液混合,其混合溶液均存在: C(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| D. | Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)=c(HCO3-)>c(H+) |
1.下列关于原电池的叙述正确的是( )
| A. | 原电池是化学能转变为电能的装置 | |
| B. | 构成原电池的正极和负极必须是两种不同的金属 | |
| C. | 原电池工作时,溶液中的阳离子向负极移动 | |
| D. | 原电池放电时,电子由负极经溶液到正极 |
2.在熔化状态下不导电,溶于水能完全电离的电解质是( )
| A. | NaCl | B. | HClO | C. | SO3 | D. | HClO4 |

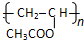 .
.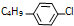 ,则R有4种.
,则R有4种.