题目内容
【题目】铁镍蓄电池又称爱迪生电池,放电时的总反应为![]() ,下列有关该电池的说法错误的是( )
,下列有关该电池的说法错误的是( )
A.电池的电解液为碱性溶液,正极为![]() 、负极为
、负极为![]()
B.电池放电时,正极反应为![]()
C.电池充电过程中,阴极附近溶液的![]() 升高
升高
D.电池充电时,阳极反应为![]()
【答案】B
【解析】
A. 放电时,Fe失电子作负极、正极为Ni2O3,Fe和Ni2O3都生成氢氧化物,说明溶液呈碱性,故A正确;
B. 放电时,Fe失电子和氢氧根离子反应生成氢氧化亚铁,负极电极反应式为Fe+2OH2e═Fe(OH)2,故B错误;
C. 充电过程中,阴极反应式为Fe(OH)2+2e═Fe+2OH,有氢氧根离子生成,所以溶液的pH增大,故C正确;
D. 充电时,阳极上失电子发生氧化反应,电极反应式为2Ni(OH)2+2OH2e═Ni2O3+3H2O,故D正确;
答案选B。

 全能测控期末小状元系列答案
全能测控期末小状元系列答案【题目】应用酸碱中和滴定原理测定某市售白醋的含量。
I.实验步骤
(I)量取10.00mL食用白醋,稀释到100mL,得到待测白醋溶液,取待测白醋溶液20.00mL于锥形瓶中,向其中滴加几滴________作指示剂。
(2)碱式滴定管盛装0.1000mol/LNaOH溶液初始时的液面位置如图所示,此时的读数_____mL。
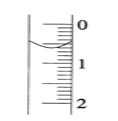
(3)滴定过程中,滴至_________________时即为滴定终点,记录NaOH溶液的最终读数。重复滴定4次。
Ⅱ.实验记录
实验序号 | 待测白醋溶液体积/mL | 0.1000mol/LNaOH溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 20.00 | 0.10 | l5.10 |
2 | 20.00 | 0.00 | 14.95 |
3 | 20.00 | 0.15 | 15.20 |
4 | 20.00 | 1.10 | 17.10 |
Ⅲ.数据处理与讨论
(4)按实验所得数据,可折算得c(市售白醋)=__________mol/L。
(5)在本实验的滴定过程中,下列操作会使实验结果偏大的是________(填选项字母)。
a.碱式滴定管在装液前未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气池,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
