题目内容
第二周期元素,能与氧形成X2O5.则有关X的叙述正确的是( )
| A、X的单质在常温下以分子晶体形式存在 |
| B、X2O5的水化物是一种强酸 |
| C、X的氢化物在固态属于离子晶体 |
| D、X所在族元素的单质在固态时都属于同一晶体类型 |
考点:元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:第二周期元素,能与氧形成X2O5.则元素的化合价为+5价,为N元素,以此来解答.
解答:
解:第二周期元素,能与氧形成X2O5.则元素的化合价为+5价,为N元素,
A.氮气常温下为气体,不能形成分子晶体,故A错误;
B.X2O5的水化物为硝酸,是一种强酸,故B正确;
C.X的氢化物为氨气,在固态属于分子晶体,故C错误;
D.X所在族元素的单质在固态时,N、P、As的单质为分子晶体,而Sb、Bi的单质为金属晶体,故D错误;
故选B.
A.氮气常温下为气体,不能形成分子晶体,故A错误;
B.X2O5的水化物为硝酸,是一种强酸,故B正确;
C.X的氢化物为氨气,在固态属于分子晶体,故C错误;
D.X所在族元素的单质在固态时,N、P、As的单质为分子晶体,而Sb、Bi的单质为金属晶体,故D错误;
故选B.
点评:本题考查元素周期表的结构及应用,为高频考点,把握元素的化合价与元素位置的关系推断元素为解答的关键,题目难度不大.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目
我国稀土资源丰富.下列有关稀土元素
Ce、
Ce的说法正确的是( )
136 58 |
138 58 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
实验室用于检验盐酸和其他电离时能产生Cl-的化合物的试剂是( )
| A、稀盐酸和石灰水 |
| B、氢氧化铁 |
| C、氯化钡溶液和稀硝酸 |
| D、硝酸银溶液和稀硝酸 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA |
| B、常温常压下,64g S02含有的原子总数为3NA |
| C、标准状况下,11.2L SO3中含有分子的数目为0.5NA |
| D、常温常压下,1mol Na2O2中阴离子数为2NA |
aXn-和bYm+是由短周期元素形成的最简单离子,已知Xn-比Ym+多两个电子层,下列说法中正确的是( )
| A、X只能是第三周期元素 |
| B、Y不可能是第二周期元素 |
| C、Y一定是氢元素 |
| D、a-b+n+m等于10或16 |
同周期的X、Y、Z三种元素,已知最高价氧化物的水化物酸性由强到弱顺序为HXO4>H2YO4>H3ZO4,则下列判断错误的是( )
| A、原子序数:X>Y>Z |
| B、非金属性:X>Y>Z |
| C、原子半径:X>Y>Z |
| D、气态氢化物的稳定性:HX>H2Y>ZH3 |
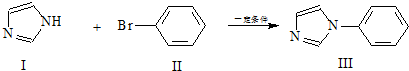
 ,Ⅴ与氢氧化钠醇溶液加热条件下反应的方程式为:
,Ⅴ与氢氧化钠醇溶液加热条件下反应的方程式为: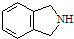 与
与 也可以发生类似反应①的反应,参加反应的分子数为2:1,则生成的产物的结构简式为
也可以发生类似反应①的反应,参加反应的分子数为2:1,则生成的产物的结构简式为