��Ŀ����
����Ŀ��ij��ɫ�����ĩ��Ʒ���ܺ���Fe2O3��Cu2O�е�һ�ֻ����֣�ijУ��ѧ����̽��ʵ��С���������ɽ���̽����
�������ϣ�Cu2O��������Һ�лᷢ����Ӧ��Cu2O+2H+=Cu+Cu2++H2O
̽��һ������ͼ��ʾװ�ý���ʵ�飬�ش��������⣺
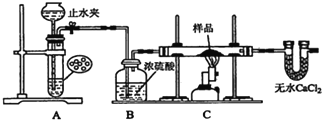
��1��������װ��ɺк�ֹˮ�У�_____����˵��װ��A�����������ã�
��2��װ��A�������ķ���װ�ã�����ѡ�õ�ҩƷ��________����ѡ�
A��ϡ�����пƬB��ϡ�������Ƭ C������������Һ����ƬD��Ũ�����þƬ
��3��������ʵ�鲽���У�ѡ����ȷ�IJ���˳��________�ۣ�����ţ�.
�ٴ�ֹˮ����Ϩ��C���ľƾ���� ��C����ȴ�����ºر�ֹˮ��
�ܵ�ȼC���ľƾ���� ���ռ��������鴿��ͨ������һ��ʱ�䣬�ž�װ���ڵĿ���
̽������
��4����ͬѧȡ������Ʒ���Թ��У�����������ϡ���ᣬ����ɫ�������ɣ���˵����Ʒ�в���Cu2O����ͬѧ��Ϊ�۵㲻��ȷ����ԭ����_____________����ͬѧ��ȡ������Ʒ���Թ��У�����������Ũ���ᣬ��������ɫ�����壮֤����Ʒ��һ������________���䷴Ӧ�����ӷ���ʽΪ_____����ͬѧԤ���ʵ��֤����һ�������Ƿ���ڣ��䷽��Ϊ__________��
��5��ȡһ������Ʒ���ձ��У�����������ϡ���ᣬ����Ӧ���˵õ�����3.2g����Һ��Fe2+��1.0mol������Ʒ��n��Cu2O��=_________mol��
���𰸡� ��װ��A�еij���©����ע��Һ�����γ�һ��Һ������Һ���߶ȱ��ֲ��� AC �ޢݢܢ� ���ɵ�ͭ�������ӷ�Ӧ Cu2O Cu2O+6H++2NO3-=2Cu2++2NO2+3H2O ȡ��ͬѧ��Ӧ�����Һ��KSCN��Һ������Һ���ɫ������ڣ�������죬���� 0.55
����������1��������װ��ɺк�ֹˮ�У���װ��A�еij���©����ע��Һ�����γ�һ��Һ������Һ���߶ȱ��ֲ��䣬��˵��װ��A��������������
��2��װ��AΪ��Һ�������ͣ�ϡ�����пƬ��Ӧ������������ϡ�������Ƭ��Ӧ����һ��������Ũ�����þƬ��Ӧ���ɶ�����������������Һ����Ƭ��Ӧ������������AC����ȷ��
��3����ʵ��ǰӦ�Ƚ�װ���ڿ����ž����鴿��ʵ�������Ӧ��Ϩ��ƾ��ƣ������������ͨ��һ��ʱ���ر�ֹˮ�У�������ȷ�IJ���˳�����٢ޢݢܢڢۡ��𰸣��ޢݢܢ�
��4������Cu2O+2H+=Cu+Cu2++H2O Fe2O3+6H+=2Fe3++3H2O Cu+2Fe3+= Cu2++2Fe2+��Ӧ��ϵ֪ͬѧ��Ϊ�۵㲻��ȷ��
��������ɫ���壬����Ӧ������![]() ��������Ʒ�к��л�ԭ�����ʣ�������
��������Ʒ�к��л�ԭ�����ʣ�������![]() ����Ӧ�Ļ�ѧ����ʽΪ
����Ӧ�Ļ�ѧ����ʽΪ![]() ��
��
Ҫ֤����Ʒ���Ƿ���![]() �����������Һ���Ƿ���
�����������Һ���Ƿ���![]() �����μӣ�
�����μӣ�![]() ��Һ������Һ��Ѫ��ɫ������Ʒ�к���
��Һ������Һ��Ѫ��ɫ������Ʒ�к���![]() ����֮����Ʒ�в���
����֮����Ʒ�в���![]() ���𰸣����ɵ�ͭ�������ӷ�Ӧ Cu2O Cu2O+6H++2NO3-=2Cu2++2NO2+3H2O ȡ��ͬѧ��Ӧ�����Һ��KSCN��Һ������Һ���ɫ������ڣ�������죬������
���𰸣����ɵ�ͭ�������ӷ�Ӧ Cu2O Cu2O+6H++2NO3-=2Cu2++2NO2+3H2O ȡ��ͬѧ��Ӧ�����Һ��KSCN��Һ������Һ���ɫ������ڣ�������죬������
��5����Һ�����η�����Ӧ�����ӷ���ʽΪ![]() ��
��![]() ��
��![]() ����Ӧ���˵õ�
����Ӧ���˵õ�![]() ����Һ��
����Һ��![]() ��
��![]() ������뷴Ӧ��
������뷴Ӧ��![]() �����Է�Ӧ������
�����Է�Ӧ������![]() �����ʵ���Ϊ
�����ʵ���Ϊ![]() ��������Ʒ��
��������Ʒ��![]() ��
��

 ������ÿ�ʱ�Ż���ҵϵ�д�
������ÿ�ʱ�Ż���ҵϵ�д�����Ŀ�����仯������������;��������ʵ������������±���ʾ��
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
�۵�/�� | 85.5 | 115.2 | >600���ֽ⣩ | 75.5 | 16.8 | 10.3 |
�е�/�� | 60.3 | 444.6 | 10.0 | 45.0 | 337.0 |
�ش��������⣺
��1����̬Feԭ�Ӽ۲���ӵĵ����Ų�ͼ���������ʽ��Ϊ__________����̬Sԭ�ӵ���ռ������ܼ��ĵ���������ͼΪ_________�Ρ�
��2�����ݼ۲���ӶԻ������ۣ�H2S��SO2��SO3����̬�����У�����ԭ�Ӽ۲���Ӷ�����ͬ���������ӵ���_________��
��3��ͼ��a��ΪS8�Ľṹ�����۵�ͷе�Ҫ�ȶ���������۵�ͷе�ߺܶ࣬��Ҫԭ��Ϊ__________��

��4����̬���������Ե�������ʽ���ڣ�����ӵ����幹��Ϊ_____�Σ����й��ۼ���������______�֣��������������д�����ͼ��b����ʾ�����۷��ӣ��÷�����Sԭ�ӵ��ӻ��������Ϊ________��
��5��FeS2����ľ�����ͼ��c����ʾ�������߳�Ϊa nm��FeS2���ʽ��ΪM�������ӵ�������ֵΪNA���侧���ܶȵļ������ʽΪ___________g��cm3��������Fe2+λ��![]() ���γɵ�������������ģ�����������ı߳�Ϊ______nm��
���γɵ�������������ģ�����������ı߳�Ϊ______nm��