题目内容
7.下列对于Na、Mg、Al的有关性质的叙述中,正确的是( )| A. | 离子的氧化性:Na+>Mg2+>Al3+ | B. | 原子半径:Al>Mg>Na | ||
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | D. | 单质的还原性:Na<Mg<Al |
分析 Na、Mg、Al位于周期表同一周期,从左到右,金属性逐渐增强,最高价氧化物对应的水化物的碱性减弱,对应的单质的还原性逐渐减弱,粒子半径逐渐减小.
解答 解:A、金属的原还性越强,对应离子的氧化性越弱,则Na+<Mg2+<Al3+,故A错误;
B、同周期原子半径从左到右逐渐减小,则原子半径:Na>Mg>Al,故B错误;
C、金属性:Na>Mg>Al,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,则碱性:NaOH>Mg(OH)2>Al(OH)3,故C正确;
D、元素的金属性越强,对应离子的还原性越强,则单质的还原性:Al<Mg<Na,故D错误.
故选C.
点评 本题考查元素周期律的递变规律,题目难度不大,注意把握周期律的递变规律,注意粒子半径的大小比较.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
18.A、B、C三种元素的核电荷数依次为a、b、c,它们的离子An+、Bn-、Cm-具有相同的电子层结构,且n>m,则下列关系正确的是( )
| A. | a>b>c | B. | a>c>b | C. | a=b+m+n | D. | a=c+n+m |
15.分别燃烧等物质的量的下列各组物质,其中消耗氧气量相等的是( )
①C2H2 与CH3CHO
②C2H2与C6H6
③C7H8与C6H12
④HCOOCH3与CH3COOH.
①C2H2 与CH3CHO
②C2H2与C6H6
③C7H8与C6H12
④HCOOCH3与CH3COOH.
| A. | ①③④ | B. | ①②③④ | C. | ①④ | D. | ②④ |
2.化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
| A. | CO2的电子式 | B. | Cl-的结构示意图: | ||
| C. | 乙烯的结构简式C2H4 | D. | Z质量数为37的氯原子${\;}_{37}^{17}$Cl |
16.下面是某研究小组研究的关于不同催化剂对H2O2 分解反应的催化效率.
(1)写出H2O2 在催化剂作用下分解反应的化学方程式2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
(2)从上表可以得出:活性炭、FeCl3、KI 和MnO2(粉末状)几种催化剂中,催化效率由大到小的顺序是MnO2(粉末状)>FeCl3>KI>活性炭,等质量的固体催化剂,颗粒大小对催化效率有什么影响颗粒越小催化效果越好.
(3)实验发现新鲜的动物肝脏对H2O2 的分解也有显著的催化作用,但当往溶液中加入盐酸,或给溶液加热时,就会失去催化能力,合理的解释是催化剂失去活性.
| 催化剂(0.1g) | 活性炭 | FeCl3 | KI | MnO2颗粒状 | MnO2粉末状 |
| 前15s产生氧气的量(ml)[来 | 5 | 11 | 7 | 8[ | 11 |
| 前30s产生氧气的量(ml) | 8 | 16 | 11 | 11 | 21 |
| 前45s产生氧气的量(ml) | 11 | 20 | 15 | 18 | 35 |
| 前60s产生氧气的量(ml) | 15 | 24 | 20 | 26 | 49 |
(2)从上表可以得出:活性炭、FeCl3、KI 和MnO2(粉末状)几种催化剂中,催化效率由大到小的顺序是MnO2(粉末状)>FeCl3>KI>活性炭,等质量的固体催化剂,颗粒大小对催化效率有什么影响颗粒越小催化效果越好.
(3)实验发现新鲜的动物肝脏对H2O2 的分解也有显著的催化作用,但当往溶液中加入盐酸,或给溶液加热时,就会失去催化能力,合理的解释是催化剂失去活性.
 已知甲、乙、丙、丁、戊是中学化学中常见的物质,常温下,戊是一种无色无味的液体,它们之间有如下反应关系.
已知甲、乙、丙、丁、戊是中学化学中常见的物质,常温下,戊是一种无色无味的液体,它们之间有如下反应关系.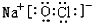 .
. .
.
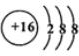 ;
;