题目内容
【题目】I.在最新的家用汽车的调查中发现,新车中气体的质量不符合标准.汽车污染主要来源于汽车配件及材料,它们都会产生大量的有毒有机物.其中一种有毒物质A,为了测定有机物A的结构,做如下实验:
①将9.2g该有机物完全燃烧,生成标况下15.68L的CO2和7.2g水;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
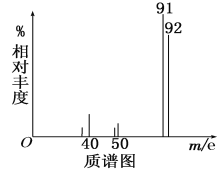
则由图可知该分子的相对分子质量是________,有机物A的分子式为_________。
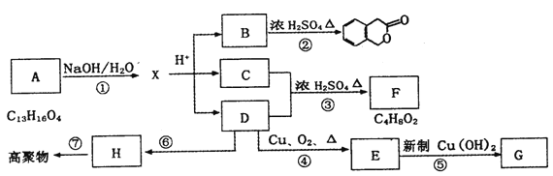
II. 已知:A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平;由A通过聚合反应生成高分子化合物F,F可用于工业合成塑料,现以A为主要原料合成G,以A为原料的合成路线如下图所示。回答下列问题:

(1)写出②、④ 、⑤两步反应的化学方程式,并注明反应类型:
②_____________________,反应类型__________。
④______________________,反应类型_________。
⑤_______________________,反应类型_________。
(2)写出由C与新制氢氧化铜反应的化学方程式及实验现象:_________________;_______________。
【答案】92 C7H8 2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O 氧化反应 CH3COOH+C2H5OH
2CH3CHO+2H2O 氧化反应 CH3COOH+C2H5OH ![]() CH3COOC2H5+H2O 酯化反应 CH3COOCH2CH3+NaOH
CH3COOC2H5+H2O 酯化反应 CH3COOCH2CH3+NaOH ![]() CH3COONa+CH3CH2OH 水解反应 CH3CHO+2Cu(OH)2+NaOH
CH3COONa+CH3CH2OH 水解反应 CH3CHO+2Cu(OH)2+NaOH![]() CH3COONa+Cu2O↓+3H2O 有砖红色沉淀生成
CH3COONa+Cu2O↓+3H2O 有砖红色沉淀生成
【解析】
I.质谱图中最右边的那个峰就是该物质的相对分子质量,由商余法确定其分子式;
II.A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2,与水发生加成反应生成B为CH3CH2OH,乙醇氧化生成C为CH3CHO,CH3CHO进一步氧化可得D为CH3COOH,E是一种无色透明、有香味的油状液体,CH3COOH与CH3CH2OH发生酯化反应生成G为CH3COOCH2CH3,在氢氧化钠溶液中水解生成乙醇和乙酸钠,F为高分子化合物,乙烯发生加聚反应生成F为![]() ,结合有机物的结构和性质解答该题。
,结合有机物的结构和性质解答该题。
I.(1)从质谱图中可以看出该气体的相对分子质量为92,由商余法确定其分子式:![]() =7
=7![]() 8,碳原子个数为7,氢原子个数为8,分子式为C7H8;故答案为:92;C7H8;
8,碳原子个数为7,氢原子个数为8,分子式为C7H8;故答案为:92;C7H8;
II.(1)反应②为CH3CH2OH氧化生成CH3CHO,化学方程式为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O,是氧化反应,故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O,是氧化反应,故答案为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O;氧化反应;
2CH3CHO+2H2O;氧化反应;
反应④为CH3CH2OH和CH3COOH发生酯化反应生成CH3COOCH2CH3,化学方程式为:CH3COOH+C2H5OH![]() CH3COOC2H5+H2O,是酯化反应,故答案为:CH3COOH+C2H5OH
CH3COOC2H5+H2O,是酯化反应,故答案为:CH3COOH+C2H5OH![]() CH3COOC2H5+H2O;酯化反应;
CH3COOC2H5+H2O;酯化反应;
反应⑤为CH3COOCH2CH3在NaOH溶液中水解生成乙醇和乙酸钠,化学方程式为:CH3COOCH2CH3+NaOH![]() CH3COONa+CH3CH2OH,是水解反应,故答案为:CH3COOCH2CH3+NaOHimg src="http://thumb.zyjl.cn/questionBank/Upload/2020/07/21/23/71c96e4b/SYS202007212309207872433247_DA/SYS202007212309207872433247_DA.003.png" width="43" height="21" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />CH3COONa+CH3CH2OH;水解反应;
CH3COONa+CH3CH2OH,是水解反应,故答案为:CH3COOCH2CH3+NaOHimg src="http://thumb.zyjl.cn/questionBank/Upload/2020/07/21/23/71c96e4b/SYS202007212309207872433247_DA/SYS202007212309207872433247_DA.003.png" width="43" height="21" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />CH3COONa+CH3CH2OH;水解反应;
(2)C为CH3CHO,其与新制氢氧化铜反应的化学方程式为:CH3CHO+2Cu(OH)2+NaOH![]() CH3COONa+Cu2O↓+3H2O,实验现象为有砖红色沉淀生成,故答案为:CH3CHO+2Cu(OH)2+NaOH
CH3COONa+Cu2O↓+3H2O,实验现象为有砖红色沉淀生成,故答案为:CH3CHO+2Cu(OH)2+NaOH![]() CH3COONa+Cu2O↓+3H2O;有砖红色沉淀生成。
CH3COONa+Cu2O↓+3H2O;有砖红色沉淀生成。

 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案