题目内容
【题目】氨和硝酸都是重要的工业原料。
(1)标准状况下,将500L氨气溶于水形成1L氨水,则此氨水的物质的量浓度为____mol·L-1(保留三位有效数字)。工业上常用过量氨水吸收二氧化硫,该反应的化学方程式为____。
(2)氨氧化法是工业生产中合成硝酸的主要途径。合成的第一步是将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮,该反应的化学方程式为____。
下列反应中的氨与氨氧化法中的氨作用相同的是____。
A.2Na+2NH3=2NaNH2+H2↑ B.2NH3+3CuO=3Cu+N2+3H2O
C.4NH3+6NO=5N2+6H2O D.HNO3+NH3=NH4NO3
工业中的尾气(假设只有NO和NO2)用烧碱进行吸收,反应的离子方程式为2NO2+2OH-=NO2-+NO3-+H2O和NO+NO2+2OH-=____+H2O(配平该方程式)。
(3)向27.2gCu和Cu2O的混合物中加入某浓度的稀HNO3500mL,反应过程中产生的气体只有NO。固体完全溶解后,在所得溶液(金属阳离子只有Cu2+)中加入1L1mol·L-1的NaOH溶液使金属离子恰好完全沉淀,此时溶液呈中性,所得沉淀质量为39.2g。
①Cu与稀HNO3反应的离子方程式为____。
②Cu与Cu2O的物质的量之比为____。
③HNO3的物质的量浓度为____mol·L-1。
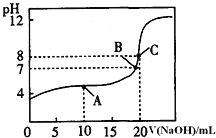
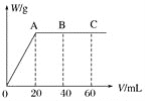
(4)有H2SO4和HNO3的混合溶液20mL,加入0.25molL-1Ba(OH)2溶液时,生成沉淀的质量w(g)和Ba(OH)2溶液的体积V(mL)的关系如图所示(C点混合液呈中性)。则原混合液中H2SO4的物质的量浓度为____mol·L-1,HNO3的物质的量浓度为____mol·L-1。
【答案】22.3 SO2+2NH3H2O=(NH4)2SO3+H2O[或SO2+2NH3+H2O=(NH4)2SO3] 4NH3+5O2![]() 4NO+6H2O BC 2NO2- 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O 2:1 2.4 0.25 1
4NO+6H2O BC 2NO2- 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O 2:1 2.4 0.25 1
【解析】
(1)根据c=![]() 计算氨水的浓度;
计算氨水的浓度;
(2)根据已知信息反:应物和生成物书写反应方程式,根据电子守恒配平反应方程式;根据化合价变化判断NH3为还原剂,进行分析其他几反应中氨气的作用;
(3)根据质量守恒,原子守恒、电子守恒规律进行解答;
(4)根据n(H+)=n(OH-)进行分析解答。
(1)标准状况下,将500L氨气溶于水形成1L氨水,则此氨水的物质的量浓度为C=![]() =
= =22.3 mol·L-1。工业上常用过量氨水吸收二氧化硫,二氧化硫与氨气反应生成亚硫酸铵和水,该反应的化学方程式为SO2+2NH3H2O=(NH4)2SO3+H2O[或SO2+2NH3+H2O=(NH4)2SO3],所以答案为:22.3;SO2+2NH3H2O=(NH4)2SO3+H2O[或SO2+2NH3+H2O=(NH4)2SO3];
=22.3 mol·L-1。工业上常用过量氨水吸收二氧化硫,二氧化硫与氨气反应生成亚硫酸铵和水,该反应的化学方程式为SO2+2NH3H2O=(NH4)2SO3+H2O[或SO2+2NH3+H2O=(NH4)2SO3],所以答案为:22.3;SO2+2NH3H2O=(NH4)2SO3+H2O[或SO2+2NH3+H2O=(NH4)2SO3];
(2)将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮,该反应的化学方程式为4NH3+5O2![]() 4NO+6H2O,所以答案:4NH3+5O2
4NO+6H2O,所以答案:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
A.在4NH3+5O2![]() 4NO+6H2O反应中,氨气做还原剂,2Na+2NH3=2NaNH2+H2↑反应中,氨气做氧化剂,所以与氨氧化法中的氨作用不相同,故A错误;
4NO+6H2O反应中,氨气做还原剂,2Na+2NH3=2NaNH2+H2↑反应中,氨气做氧化剂,所以与氨氧化法中的氨作用不相同,故A错误;
B.在2NH3+3CuO=3Cu+N2+3H2O反应中,氨气做还原剂,所以与氨氧化法中的氨作用相同,故B正确;
C.在4NH3+6NO=5N2+6H2O反应中,氨气做还原剂,所以与氨氧化法中的氨作用相同,故C正确;
D.HNO3+NH3=NH4NO3反应是非氧化还原反应,故D错误;
所以答案:BC。
由质量守恒和得失电子守恒配平,NO中N为+2价,NO2中N为+4,显然是个归中反应,生成化合物中N为+3价,再根据原子守恒,电荷守恒,可知该反应的离子方程式: NO+NO2+2OH-=2NO2-+H2O,故答案为NO2-;
本题答案为:4NH3+5O2![]() 4NO+6H2O;BC;2NO2-;
4NO+6H2O;BC;2NO2-;
(3)向27.2gCu和Cu2O的混合物中加入某浓度的稀HNO3500mL,反应过程中产生的气体只有NO。固体完全溶解后,在所得溶液(金属阳离子只有Cu2+)中加入1L1mol·L-1的NaOH溶液使金属离子恰好完全沉淀,此时溶液呈中性,所得沉淀质量为39.2g。
①Cu与稀HNO3反应生成硝酸铜、一氧化氮和水,其离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,所以答案:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
②所得溶液中加入1mol/L的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,溶液中溶质为NaNO3,n(NaNO3)=n(NaOH)=1.0mol/L![]() 1.0L=1mol。沉淀为Cu(OH)2,质量为39.2g,物质的量=
1.0L=1mol。沉淀为Cu(OH)2,质量为39.2g,物质的量=![]() =0.4mol,根据铜元素守恒有n(Cu)+2n(Cu2O)=n[Cu(OH)2],反应后的溶液中n[Cu(NO3)2]=n[Cu(OH)2]=0.4mol。设Cu、Cu2O的物质的量分别为x、y,64x+144y=27.2, x+2y=0.4,解得x=0.2,y=0.1,所以Cu与Cu2O的物质的量之比为2:1;所以答案为2:1;
=0.4mol,根据铜元素守恒有n(Cu)+2n(Cu2O)=n[Cu(OH)2],反应后的溶液中n[Cu(NO3)2]=n[Cu(OH)2]=0.4mol。设Cu、Cu2O的物质的量分别为x、y,64x+144y=27.2, x+2y=0.4,解得x=0.2,y=0.1,所以Cu与Cu2O的物质的量之比为2:1;所以答案为2:1;
③Cu和Cu2O与稀硝酸反应生成硝酸铜,0.2molCu完全反应失去0.4mol电子0.1molCu2O完全反应失去0.2mol电子,总共生成0.6mol电子,由电子守恒,生成NO的物质的量=![]() =0.2mol,所得溶液中加入1L1mol·L-1的NaOH溶液,此时溶液呈中性,金属离子恰好完全沉淀,反应后的溶质为硝酸钠,则溶液中的硝酸根离子的物质的量为
=0.2mol,所得溶液中加入1L1mol·L-1的NaOH溶液,此时溶液呈中性,金属离子恰好完全沉淀,反应后的溶质为硝酸钠,则溶液中的硝酸根离子的物质的量为
n(NO3-)=n(NaOH)=1mol/L![]() 1L=1mol,则硝酸的总物质的量为1mol+0.2mol=1.2mol,硝酸的浓度c=
1L=1mol,则硝酸的总物质的量为1mol+0.2mol=1.2mol,硝酸的浓度c=![]() =2.4mol/L。所以答案为:2.4 mol·L-1。
=2.4mol/L。所以答案为:2.4 mol·L-1。
(4)由图可知,0~20mLBa(OH)2溶液发生H2SO4+Ba(OH)2=BaSO4↓+H2O,20mL~60mLBa(OH)2溶液发生H++OH-=H2O,由图可知,加入20mLBa(OH)2溶液时,硫酸钡沉淀达最大值,设硫酸的物质的量为x,则
H2SO4+Ba(OH)2=BaSO4↓+ H2O
1 1
x 0.02L![]() 0.25mol
0.25mol![]() L-1,解得x=0.02L
L-1,解得x=0.02L![]() 0.25mol
0.25mol![]() L-1=0.005mol,硫酸的物质的量浓度=
L-1=0.005mol,硫酸的物质的量浓度=![]() =0.25 mol
=0.25 mol![]() L-1,由图可知pH=7时,消耗60mLBa(OH)2溶液,由.H++OH-=H2O可知原溶液中含有的n(H+)=n(OH-)=2
L-1,由图可知pH=7时,消耗60mLBa(OH)2溶液,由.H++OH-=H2O可知原溶液中含有的n(H+)=n(OH-)=2![]() 0.06L
0.06L![]() 0.25 mol
0.25 mol![]() L-1=0.03mol,故
L-1=0.03mol,故
n(HNO3)=0.03mol-0.005mol![]() 2=0.02mol,故原溶液中HNO3的物质的量浓度=
2=0.02mol,故原溶液中HNO3的物质的量浓度=![]() =1 mol
=1 mol![]() L-1,故答案为:0.25;1。
L-1,故答案为:0.25;1。

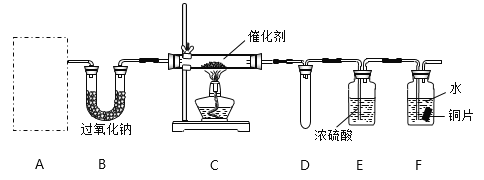
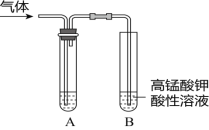
【题目】Ⅰ.实验室制得气体中常含有杂质,影响其性质的检验。下图A为除杂装置,B为性质检验装置,完成下列表格:
序号 | 气体 | 反应原理 | A中试剂 |
① | 乙烯 | 无水乙醇与浓硫酸共热,反应的化学方程式是______ | ___ |
② | 乙烯 | 溴乙烷与NaOH的乙醇溶液共热,反应的化学方程式是_____ | ___ |
③ | 乙炔 | 向电石中滴加饱和食盐水,反应的化学方程式是___ | ____ |
Ⅱ.为探究乙酸乙酯的水解情况,某同学取大小相同的3支试管,分别加入以下溶液,充分振荡,放在同一水浴中加热相同时间,观察到如下现象。
试管编号 | ① | ② | ③ |
实验操作 |
|
|
|
实验现象 | 酯层变薄 | 酯层消失 | 酯层基本不变 |
(1)试管②中反应的化学方程式是__________。
(2)设计试管③实验的作用是__________。
(3)实验结论是__________。