��Ŀ����
5��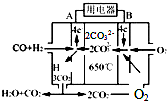 �о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ��������õķ���������Ҫ���壮
�о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ��������õķ���������Ҫ���壮��1��һ�������£�NO2��SO2��Ӧ����SO3��NO�������壮�������Ϊ1��2��NO2��SO2���������ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����bc��
a����ϵѹǿ���ֲ��� b�����������ɫ���ֲ���
c����ϵ��SO3������������ֲ��� d��ÿ����1mol SO2��ͬʱ����1molNO
��2�����������Ӧƽ��ʱNO2��SO2�����Ϊ1��6����ƽ�ⳣ��K=$\frac{8}{3}$��
��3�����Ͱ��������������Ļ�ѧԭ���Dz��ð�ˮ���������е�SO2������һ�������������������ղ��ﷴӦ���ü������ŵ�����ܻ�������SO2�⣬���ܵõ�һ�ָ��Ϸ��ϣ��ø��Ϸ��Ͽ��ܵĻ�ѧʽΪ��NH4��3PO4����NH4��2HPO4��NH4H2PO4����д��һ�ּ��ɣ���
��4����ͼ��MCFCȼ�ϵ�أ�������ˮú����CO��H2��
Ϊȼ�ϣ�һ������Li2CO3��Na2CO3���ۻ����Ϊ����ʣ�AΪ��صĸ�����ѡ�����������д��B���缫��Ӧʽ2CO2+O2+4e-=2CO32-��
��5����ҵ�ϳ���Na2CO3��Һ���շ����������������NO��NO2�Ļ����Ϊ������
��֪��NO������Na2CO3��Һ��Ӧ��
NO+NO2+Na2CO3=2NaNO2+CO2
2NO2+Na2CO3=NaNO2+NaNO3+CO2
����������Na2CO3��Һ��ȫ����NO��NO2�Ļ���ÿ����22.4L����״����CO2��ȫ���ݳ���ʱ������Һ����������44g������������NO��NO2�������Ϊ1��7��
����Na2CO3��Һ���շ�����������������ڵ�ȱ���Ǻ�NO�϶�����������ȫ���գ�
���� ��1��a���淴Ӧ��NO2��g��+SO2��g��?SO3��g��+NO��g���Ľ��У�������ܵ����ʵ������䣬ѹǿ���䣮
b�����������ɫ���ֲ��䣬˵������������Ũ�Ȳ��䣮
c���淴Ӧ����NO��O2�����ʵ���֮�ȷ����仯��
d��ÿ����1mol SO2��ͬʱ����1mol NO����ʾ����Ӧ���ʣ�
��2��������ʽ��������ʵ�Ũ���Լ���ѧƽ�ⳣ������ʽ���㻯ѧƽ�ⳣ����
��3�������Ǽ������壬���Ժ��ᷴӦ�����Σ�
��4��̼����ȼ�ϵ����ͨ�����ĵ缫һ��Ϊ������ͨ��ȼ�ϵĵ缫һ��Ϊ�����������ڸõ缫�Ϸ�����ԭ��Ӧ��
��5���ٸ��ݶ�����̼�����������Һ�������ӵ����з�������һ�������Ͷ���������������Ӷ��ó������֮�ȣ�
�ڸ��ݹ����NO������Na2CO3��Һ��Ӧ��
��� �⣺��1��a���淴Ӧ���У���������ʵ������䣬ѹǿ���䣬��ϵѹǿ���ֲ��䣬����˵������ƽ��״̬����a����
b�����������ɫ���ֲ��䣬˵������������Ũ�Ȳ��䣬˵������ƽ��״̬����b��ȷ��
c���淴Ӧ����NO��O2�����ʵ���֮�ȷ����仯��NO��O2�����ʵ���֮�ȱ��ֲ��䣬˵������ƽ��״̬����c��ȷ��
d��ÿ����1mol SO2��ͬʱ����1mol NO����ʾ����Ӧ���ʣ���Ӧ��ʼ���ն����˱������У���d����
��ѡ��bc��
��2��NO2��g��+SO2��g��?SO3��g��+NO��g��
��ʼ���ʵ���� a 2a 0 0
ת�����ʵ���� x x x x
ƽ�����ʵ���� a-x 2a-x x x
ƽ��ʱNO2��SO2�����Ϊ1��6������1a-x������2a-x��=1��6����x=$\frac{4}{5}$a����ƽ�ⳣ��K=$\frac{C��SO{\;}_{3}��C��NO��}{c��NO{\;}_{2}��C��SO{\;}_{2}��}$=$\frac{x{\;}^{2}}{��a-x����2a-x��}$=$\frac{\frac{16}{25}a{\;}^{2}}{\frac{1}{5}a��\frac{6}{5}a}$=$\frac{8}{3}$��
�ʴ�Ϊ��$\frac{8}{3}$��
��3�������Ǽ������壬���Ժ����ᷴӦ�����Σ������������������������Ķ��ٶ���ͬ�����Բ�������泥�������炙����������泥��ʴ�Ϊ����NH4��3PO4����NH4��2HPO4��NH4H2PO4����
��4��̼����ȼ�ϵ����ͨ�����ĵ缫һ��Ϊ������ͨ��ȼ�ϵĵ缫һ��Ϊ�����������ڸõ缫�Ϸ�����ԭ��Ӧ���ʴ�Ϊ������2CO2+O2+4e-=2CO32-��
��5������NO�����ʵ�����x��NO2�����ʵ�����y����
x+$\frac{y-x}{2}$=$\frac{22.4}{22.4}$mol��
32x+24��y-x��=44
��ã�x=$\frac{1}{4}$��y=$\frac{7}{4}$����һ�������Ͷ������������ʵ���֮��$\frac{1}{4}$��$\frac{7}{4}$=1��7��������ͬ�����£�һ�������Ͷ������������֮����1��7���ʴ�Ϊ��1��7��
��NO������Na2CO3��Һ��Ӧ�����Զ��ں�NO�϶�����������ȫ���գ��ʴ�Ϊ����NO�϶�����������ȫ���գ�
���� ������Ҫ����ƽ��״̬�жϡ�ƽ�ⳣ�����缫��Ӧ�Լ���ѧ���㣬ע��ƽʱ֪ʶ�Ļ����Լ����Ӧ���ǽ���Ĺؼ����ѶȲ���

| A�� | 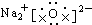 | B�� | 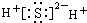 | ||
| C�� | 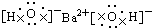 | D�� |  |
| A�� | Ba��OH��2��Һ | B�� | NaOH��Һ | C�� | KNO3��Һ | D�� | AgNO3��Һ |
| A�� | �ڱ�״���£���4molHCl��Ũ������������MnO2��Ӧ������22.4L���� | |
| B�� | ��״���£�2.24L H2O�к���H2O������Ϊ0.1NA | |
| C�� | 1L 0.1mol/L NaHSO4��Һ�к��е���������ĿΪ0.1NA | |
| D�� | ʵ�������Ƶõ�1.7g NH3�к��еĵ�����ΪNA |
| A�� | ��֪������AgCl���ܽ��Զ����AgBr���ֽ�AgCl��AgBr�����ֱ�����Һ�������Ϻ��ټ�������ŨAgNO3��Һ�����ɵ�AgCl��������AgBr���� | |
| B�� | Fe��OH��3�������������ӷ���ʽΪ��Fe��OH��3+3H+=Fe3++3H2O | |
| C�� | ���ȳʻ�ɫ����Һ�У�I-��Cl-��NO3-��Na+һ�����Դ������� | |
| D�� | ��֪�����ȼ����Ϊ890.3kJ•mol-1�����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪ�� CH4��g��+2O2��g��=CO2��g��+2H2O��g����H=-890.3kJ•mol-1 |
| A�� | CO2 | B�� | PCl3 | C�� | CCl4 | D�� | H2O |
| A�� | NaͶ�����������У�2Na+2H2O=2Na++2OH-+H2�� | |
| B�� | Cl2ͨ��ˮ�У�Cl2+H2O=2H++Cl-+ClO- | |
| C�� | ��Na2CO3��Һ�м����������CO32-+2H+=H2O+CO2�� | |
| D�� | NaHCO3��Һ�м����������ʯ��ˮ��Ca2++HCO3-+OH-=H2O+CaCO3�� |
 ��CaCl2
��CaCl2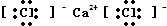 ��
��