题目内容
17.在下列分子结构中,原子的最外层电子不能满足8电子稳定结构的是( )| A. | CO2 | B. | PCl3 | C. | CCl4 | D. | H2O |
分析 根据原子最外层电子数和化合价判断,在化合物中,原子最外层电子数等于原子的价层电子数+|化合价|,以此进行分析.
解答 解:A、CO2中,C原子的最外层电子为:4+4=8,O原子的最外层电子为:6+|-2|=8,都满足8电子稳定结构,故A正确;
B、PCl3中,P原子的最外层电子为:5+3=8,Cl原子的最外层电子为:7+|-1|=8,都满足8电子稳定结构,故B正确;
C、CCl4中,C属于第IVA族元素,碳元素的族序数+成键数=4+4=8,所以该分子中所有原子最外层电子都满足8电子稳定结构,故C正确;
D、H2O中,O原子的最外层电子数为6+2=8,H原子的最外层电子数为1+1=2,不满足8电子稳定结构,故D错误;
故选:D.
点评 本题考查原子核外电子是否满足8电子稳定结构,题目难度不大,注意判断问题的角度及H原子的特殊情况.

练习册系列答案
相关题目
12.如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液构成原电池.下列叙述正确的是( )

| A. | Zn是负极,发生还原反应 | |
| B. | 一段时间后,铜片质量减轻 | |
| C. | 电流从铜片经导线流向锌片 | |
| D. | 一段时间后,电解质溶液的酸性保持不变 |
2.下列关于化学键的说法正确的是( )
| A. | 离子化合物中一定存在离子键,可能存在共价键 | |
| B. | 由金属元素和非金属元素组成的化学键一定是共价键 | |
| C. | 非极性键只存在于双原子单质分子中 | |
| D. | 不同元素组成的多原子分子里的化学键一定为极性键 |
9.下列说法中,正确的是( )
| A. | 1-丁烯和2-丁烯都存在顺反异构现象 | |
| B. | 一氯甲烷不存在同分异构体的事实可以证明甲烷分子是正四面体形分子 | |
| C. | 间二氯苯只有一种结构的事实可以证明苯分子是正六边形分子 | |
| D. | 苯不能使高锰酸钾酸性溶液或溴的四氯化碳溶液褪色可以证明苯分子中的碳碳键完全相同 |
6.NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A. | 1molFeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 2L0.5mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 1molNa2O2固体中含离子总数为4NA | |
| D. | 丙烯(CH2=CH-CH3)和环丙烷组成的42g混合气体中氢原子的个数为6NA |
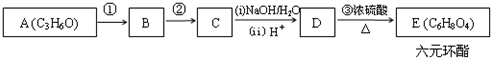
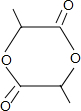 +2H2O.
+2H2O.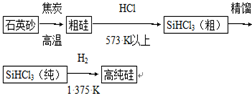
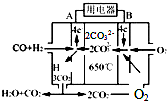 研究NO2、SO2、CO等大气污染气体的处理及利用的方法具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理及利用的方法具有重要意义.