题目内容
【题目】下列轨道表示式表示的元素原子中,能量处于最低状态的是( )
A.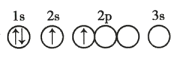 B.
B.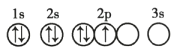
C. D.
D.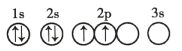
【答案】D
【解析】
洪特规则:即电子分布到能量简并的原子轨道时,优先以自旋相同的方式分别占据不同的轨道,因为这种排布方式原子的总能量最低,所以在能量相等的轨道上,电子尽可能自旋平行地多占不同的轨道;泡利不相容原理:指的是在原子中不能容纳运动状态完全相同的两个电子;能量最低原理:原子核外的电子应优先排布在能量最低的能级里,然后由里到外,依次排布在能量逐渐升高的能级里。
A.2s能级的能量比2p能量低,电子尽可能占据能量最低的轨道,不符合能量最低原理,故A错误;
B.2p能级的3个简并轨道(能级相同的轨道)只有被电子逐一自旋平行的占据后,才能容纳第二个电子,违背洪特规则,故B错误;
C.2s能级的能量比2p、3s能量低,电子尽可能占据能量最低的轨道,不符合能量最低原理,故C错误;
D.能级能量由低到高的顺序为:1s、2s、2p,每个轨道最多只能容纳两个电子,且自旋相反,简并轨道(能级相同的轨道)中电子优先单独占据1个轨道,且自旋方向相同,原子处于基态,其能量最低,故D正确;
综上所述,答案为D。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目