题目内容
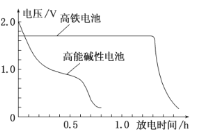
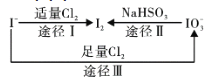
【题目】25℃时,用 0.100 mol /L 盐酸滴定 20.00 mL 0.100 mol/L的CH3COONH4溶液,滴定曲线如下图所示,下列说法正确的是( )

A.可用酚酞作滴定指示剂
B.滴定过程中水的电离程度不断增大
C.P点溶液中:2c(![]() )<3c(CH3COO-)+c(CH3COOH)
)<3c(CH3COO-)+c(CH3COOH)
D.Q点溶液中:c(Cl-)>c(![]() )>c(CH3COO-)>c(H+)
)>c(CH3COO-)>c(H+)
【答案】C
【解析】
A.盐酸和CH3COONH4溶液反应生成醋酸和氯化铵,反应终点溶液为酸性,用甲基橙作滴定指示剂,A错误;
B.滴定过程中CH3COO-的浓度减小,对水的电离促进作用减弱,水的电离程度减小,B错误;
C.P点溶液中电荷守恒:c(CH3COO-)+c(OH-)+c(Cl-)=c(NH4+)+c(H+),物料守恒:c(CH3COO-)+c(CH3COOH)=2c(Cl-),①式乘以2,和②式相加,得到:2c(H+)+2c(![]() )=3c(CH3COO-)+c(CH3COOH)+2c(OH-),P点溶液呈酸性,c(H+)>c(OH-),所以2c(
)=3c(CH3COO-)+c(CH3COOH)+2c(OH-),P点溶液呈酸性,c(H+)>c(OH-),所以2c(![]() )<3c(CH3COO-)+c(CH3COOH),C正确;
)<3c(CH3COO-)+c(CH3COOH),C正确;
D.Q点溶液中溶质为物质的量之比为1:1的醋酸和氯化铵,铵根离子水解,则c(Cl-)>c(![]() ),因醋酸电离程度小且水也电离出氢离子,则c(
),因醋酸电离程度小且水也电离出氢离子,则c(![]() )>c(H+)>c(CH3COO-),所以c(Cl-)>c(
)>c(H+)>c(CH3COO-),所以c(Cl-)>c(![]() )>c(H+)>c(CH3COO-),D错误;
)>c(H+)>c(CH3COO-),D错误;
故选C。

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案【题目】硼氢化钠(NaBH4)是常用的还原剂,用途广泛。某探究小组采用偏硼酸钠(NaBO2)为主要原料制备NaBH4,其流程如下:
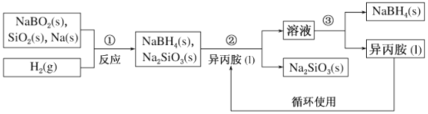
已知:NaBH4常温下易与水反应,可溶于异丙胺(沸点:33℃)
(1)在第①步反应加料之前,需要将反应器加热至 100 ℃以上并通入氩气 ,该操作的目的是______;第②步分离采用的方法是______;第③步分离NaBH4并回收溶剂,采用的方法是_____;
(2)NaBH4与水反应生成H2 : NaBH4 + 2H2O=NaBO2+4H2↑ (已知:HBO2是弱酸)。 实验测得,NaBH4每消耗一半所用的时间与溶液 pH、温度的关系如下表:
pH | 8 | 10 | 12 | 1 4 |
温度/℃ | 25 | 25 | 25 | 25 |
时间/ min | 6. 2 ×10-1 | 6. 2 ×10 | 6. 2 ×103 | 6. 2 ×105 |
①NaBH4与水反应开始释放H2很快 ,经过一段时间后就缓慢下来 ,可能原因一是反应物浓度降低 ;二是________;
②为了加快制取的H2速率,常将一些促进剂投入水中,下列物质中可作为促进剂的是__;
a. 碳酸钾 b. 稀硝酸 c 硫酸氢钠 d. 氨水
(3)利用如图所示装置,可以测定NaBH4与水反应生成 H2的速率,在pH =10、25℃条件下,将恒压滴液漏斗中NaBH4滴加到含有催化剂的三颈烧瓶中。
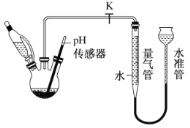
①实验中使用恒压滴液漏斗的原因为_________;
②气体生成结束后,水准管中的液面会高于量气管中的液面,此时量气管读数会_____( 填“偏大”或“偏小”)需要将水准管慢慢向下移动,则量气管中的液面会__________(填“上升”或“下降”);
③在此条件下,0. 38 g NaBH4开始反应至剩余 0. 19 g 时,实验测得量气管内气体体积为124mL,则这段时间内,生成H2的平均速率是_______mL·min-1。