题目内容
【题目】(1)甲基的电子式 ,氢元素含量最高的烃的分子式______________。
(2)支链只有一个乙基且相对分子质量最小的烷烃的结构简式为
(3)某炔烃经催化加氢后,得到2-甲基丁烷,该炔烃的名称是 (系统命名法命名)
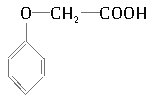
(4)已知某有机物的结构简式为:![]()
①该有机物中所含官能团的名称是________________;_______________。
②写出该有机物使溴水褪色的反应化学方程式_____________________________________
【答案】(1)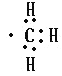 CH4;(2)
CH4;(2)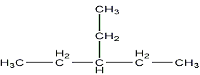 ;(3) 3-甲基-1-丁炔;
;(3) 3-甲基-1-丁炔;
(4)①碳碳双键 氯原子;②CH2=CH-CH2-Cl +Br2 ![]() CH2 Br CH Br CH2Cl.
CH2 Br CH Br CH2Cl.
【解析】
试题分析:(1)甲基的电子式为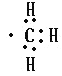 ,氢元素含量最高的烃是甲烷,分子式为CH4,答案为:
,氢元素含量最高的烃是甲烷,分子式为CH4,答案为: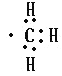 CH4;(2)支链只有一个乙基且相对分子质量最小的烷烃,根据必须选最长碳链为主链,可知该烃的名称为2-乙基戊烷,结构简式为:
CH4;(2)支链只有一个乙基且相对分子质量最小的烷烃,根据必须选最长碳链为主链,可知该烃的名称为2-乙基戊烷,结构简式为: ,答案为:
,答案为: ;(3)2-甲基丁烷的结构简式为:
;(3)2-甲基丁烷的结构简式为:![]() ,根据2-甲基丁烷的结构简式可知,该炔烃只能是3-甲基-1-丁炔,答案为:3-甲基-1-丁炔;(4)已知某有机物的结构简式为: CH2=CH—CH2—Cl,①该有机物中所含官能团有碳碳双键、氯原子,答案为:碳碳双键 氯原子;②该有机物使溴水褪色是溴单质与碳碳双键发生加成反应,反应化学方程式为:
,根据2-甲基丁烷的结构简式可知,该炔烃只能是3-甲基-1-丁炔,答案为:3-甲基-1-丁炔;(4)已知某有机物的结构简式为: CH2=CH—CH2—Cl,①该有机物中所含官能团有碳碳双键、氯原子,答案为:碳碳双键 氯原子;②该有机物使溴水褪色是溴单质与碳碳双键发生加成反应,反应化学方程式为:
CH2=CH-CH2-Cl +Br2 ![]() CH2 Br CH Br CH2Cl,答案为:CH2=CH-CH2-Cl +Br2
CH2 Br CH Br CH2Cl,答案为:CH2=CH-CH2-Cl +Br2 ![]() CH2 Br CH Br CH2Cl
CH2 Br CH Br CH2Cl

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目