��Ŀ����
A ��B��C��D��E���ֶ�����Ԫ�أ����ǵ�ԭ��������������AԪ�ص�ԭ�Ӱ뾶��С��BԪ�ص�����������Ӧˮ���������⻯����������M��D��Aͬ���壬����Eͬ���ڣ�EԪ��ԭ�ӵ������������ȴ�����������2��A��B��D��E������Ԫ�أ�ÿһ����CԪ�ض����γ�ԭ�Ӹ����Ȳ���ͬ�������ֻ������ش�
��1��C��E����Ԫ����Ƚϣ��ǽ����Խ�ǿ��Ԫ�������ڱ��е�λ��Ϊ ����������˵���У�������֤C��E�ǽ�����ǿ������ ��
a���Ƚ�������Ԫ�صij������ʵķе�
b�������γɵĻ������У�CԪ���Ը���
c���Ƚ�������Ԫ�ص���̬�⻯����ȶ���
��2����Ԫ�ط��ű�ʾB,C,D����Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ ��
��3����M�к��еĻ�ѧ��������
��B����ۺ�����N,�����£���M,N������Һ��pH������5,����ˮ�������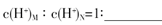
��4��DԪ�ص�����������Ӧˮ��������ؿ��к������Ľ���Ԫ���γɵĵ��ʷ�Ӧ����д���÷�Ӧ�����ӷ���ʽ �������ӷ���ʽ��ʾ�÷�Ӧ���ɵ�����Һ�Լ��Ե�ԭ��
��5��C��D��ԭ�Ӹ�����1:1�γ�һ�����ӻ�����R����֪����ʱR��ˮ��Ӧ���ָ���ԭ״̬��ã�ÿת��1 mol���ӷų�QkJ����������д��R��ˮ��Ӧ���Ȼ�ѧ��Ӧ����ʽ ��
��1���ڶ����ڢ�A�壬bc����2��N��O��Na����3�����Ӽ������ۼ���10��4��
��4��2Al + 2OH- + 2H2O=2AlO2-
+ 3H2����AlO2- + 2H2O
 Al(OH)3 + OH-��
Al(OH)3 + OH-��
��5��2Na2O2��s��+2H2O(g)=4NaOH(aq)+O2(g)��H=��2QkJ/mol��
��������
�����������������֪��A ��B��C��D��E���ֶ�����Ԫ�أ����ǵ�ԭ��������������AԪ�ص�ԭ�Ӱ뾶��С����AΪH��BԪ�ص�����������Ӧˮ���������⻯����������M����BΪN��MΪ����泥�EԪ��ԭ�ӵ������������ȴ�����������2����EΪS��D��Aͬ���壬����Eͬ���ڣ���DΪNa��A��B��D��E������Ԫ�أ�ÿһ����CԪ�ض����γ�ԭ�Ӹ����Ȳ���ͬ�������ֻ������CΪO����1��CΪO��EΪS��������ͬ���壬���ϵ��·ǽ������ڼ�������ǽ����Խ�ǿ��Ԫ��ΪO�������ڱ��е�λ��Ϊ�ڶ����ڢ�A�壬��������˵���У�������֤C��E�ǽ�����ǿ������a��Ԫ�صķǽ�����ǿ���뵥�ʵķе�ߵ��أ�����b�������γɵĻ������У���Ԫ���Ը��ۣ�˵����Ԫ�صĵõ�����������ǿ����Ԫ�صķǽ����Ա���ǿ����ȷ��c��Ԫ�ص���̬�⻯����ȶ���Խǿ��Ԫ�صķǽ�����Խǿ����ȷ��ѡbc����2��BΪN��CΪO��DΪNa������ͬ����Ԫ����������Ԫ�صĵ�һ�����ܳʵ������ƣ�����ԭ�������p���Ϊ�����״̬�����ȶ�����һ�����ܣ�N��O��NaΪ���ý�������һ��������С������Ԫ�صĵ�һ�������ɴ�С��˳��ΪN��O��Na����3����MΪ����泥����еĻ�ѧ�����������Ӽ������ۼ���������Һ�з���ˮ�ĵ��룬����������������Ũ�ȣ��������Һ�е�������ȫ������ˮ�ĵ��룬�����£�������Һ��pH������5������ˮ�������������Ũ�ȷֱ�Ϊ10��9mol/L��10��5mol/L��c(H+)HNO3��c(H+)NH4NO3=1��10��4����4������������Һ�뵥������Ӧ����ƫ�����ƺ����������ӷ���ʽΪ2Al + 2OH- + 2H2O=2AlO2-
+ 3H2���������ӷ���ʽ��ʾ�÷�Ӧ���ɵ�����Һ�Լ��Ե�ԭ��AlO2- + 2H2O
 Al(OH)3 + OH-��
��5��O��Na��ԭ�Ӹ�����1:1�γ�һ�����ӻ�����������ƣ����������Ϣд������������ˮ��Ӧ���Ȼ�ѧ��Ӧ����ʽΪ
Al(OH)3 + OH-��
��5��O��Na��ԭ�Ӹ�����1:1�γ�һ�����ӻ�����������ƣ����������Ϣд������������ˮ��Ӧ���Ȼ�ѧ��Ӧ����ʽΪ
2Na2O2��s��+2H2O(g)=4NaOH(aq)+O2(g)��H=��2QkJ/mol��
���㣺����Ԫ���ƶϡ�Ԫ�������ɼ�������ʵ����ʡ��������Һ���Ȼ�ѧ����ʽ��д��

 [��ѧ/ѡ��/���ʽṹ������]A��B��C��D��E���ֶ�����Ԫ�أ�ԭ��������������Ԫ�ض�Ӧ�ĵ��ʾ�Ϊ���壮A��C��E��Ԫ�ص�ԭ�Ӻ����ֻ��2��δ�ɶԵ��ӣ�B��EԪ�ص�ԭ������֮�͵���C��DԪ�ص�ԭ������֮�ͣ�
[��ѧ/ѡ��/���ʽṹ������]A��B��C��D��E���ֶ�����Ԫ�أ�ԭ��������������Ԫ�ض�Ӧ�ĵ��ʾ�Ϊ���壮A��C��E��Ԫ�ص�ԭ�Ӻ����ֻ��2��δ�ɶԵ��ӣ�B��EԪ�ص�ԭ������֮�͵���C��DԪ�ص�ԭ������֮�ͣ�