题目内容
10.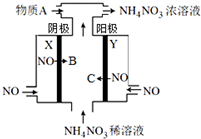 电解NO制备 NH4NO3的工作原理如图所示,X、Y皆为Pt电极,为使电解产物全部转化为NH4NO3,需补充物质A.下列说法正确的是( )
电解NO制备 NH4NO3的工作原理如图所示,X、Y皆为Pt电极,为使电解产物全部转化为NH4NO3,需补充物质A.下列说法正确的是( )| A. | 在阴极NO转化为B,B为硝酸根离子 | |
| B. | 电解一段时间,阴极附近pH升高 | |
| C. | 为使电解产物全部转化为NH4NO3,需补充的A为硝酸 | |
| D. | 该电解池的阳极反应式为:NO-3e-+4OH-=NO${\;}_{3}^{-}$+2H2O |
分析 电解NO制备NH4NO3,Y为阳极反应为NO-3e-+2H2O=NO3-+4H+,X为阴极反应为:NO+5e-+6H+=NH4++H2O,从两极反应可看出,要使得失电子守恒,阳极产生的NO3-的物质的量大于阴极产生的NH4+的物质的量,总反应方程式为8NO+7H2O$\frac{\underline{\;电解\;}}{\;}$3NH4NO3+2HNO3,因此若要使电解产物全部转化为NH4NO3,需补充NH3,据此分析.
解答 解:电解NO制备NH4NO3,Y为阳极反应为NO-3e-+2H2O=NO3-+4H+,X为阴极反应为:NO+5e-+6H+=NH4++H2O,从两极反应可看出,要使得失电子守恒,阳极产生的NO3-的物质的量大于阴极产生的NH4+的物质的量,总反应方程式为:8NO+7H2O$\frac{\underline{\;电解\;}}{\;}$3NH4NO3+2HNO3,因此若要使电解产物全部转化为NH4NO3,需补充NH3;
A.X为阴极反应为:NO+5e-+6H+=NH4++H2O,所以B为铵根离子,故A错误;
B.根据以上分析,X电极为电解池阴极,反应为:NO+5e-+6H+=NH4++H2O,消耗氢离子,则阴极附近pH升高,故B正确;
C.根据以上分析,则A为NH3,故C错误;
D.Y为阳极反应为NO-3e-+2H2O=NO3-+4H+,故D错误;
故选:B.
点评 本题考查了电解原理的应用等,题目涉及的知识点较多,侧重于考查学生的综合运用能力,难度中等,注意基础知识的积累掌握.

练习册系列答案
相关题目
20.为实现下列实验目的,所用试剂合理的是( )
| 选项 | 实验目的 | 试剂 |
| A | 除去Fe2O3中的Al2O3 | 稀盐酸 |
| B | 验证Br2的氧化性强于I2 | 溴水、KI溶液、淀粉溶液 |
| C | 检验溴乙烷中含有溴元素 | 溴乙烷、NaOH溶液、AgNO3溶液 |
| D | 制备Fe(OH)3胶体 | 饱和FeCl3溶液、NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
1.已知H3PO4为弱酸,常温下NaH2PO4溶液的pH小于7.下列关于常温下0.10mol•L-1的NaH2PO4溶液的说法正确的是( )
| A. | c(Na+)=c(H2PO4-)+c(HPO42-)+C(H3PO4) | |
| B. | c(Na+)+c(H+)=c(OH-)+c(H2PO4-)+2c(HPO42-)+3c(PO43-) | |
| C. | 温度升高,c(H2PO4-)增大 | |
| D. | 加水稀释后,m(H+)与m(OH-)的乘积不变 |
5.卤代烃在生产生活中具有广泛的应用,下列说法正确的是( )
| A. | 多氯代甲烷中分子结构为正四面体的是二氯甲烷和四氯化碳 | |
| B. | 多氯代烷常为有机溶剂,工业上分离这些多氯代物的方法是萃取 | |
| C. | 三氟氯溴乙烯(CF3CHClBr)是一种麻醉剂,有4种同分异构体(不考虑立体异构) | |
| D. | 聚氯乙烯是生活中常用的塑料,工业上以乙烯为原料经过加成、消去和聚合反应可生成聚氯乙烯 |
15.下列说法正确的是( )
| A. | 等质量的乙酸、葡萄糖与淀粉完全燃烧时消耗氧气的质量相等 | |
| B. | 醇、醛和羧酸都溶于水,烃与酯的密度都小于1g/cm3 | |
| C. | 豆浆中富含大豆蛋白,煮沸后蛋白质水解成了氨基酸 | |
| D. | 某烯烃(最简式为CH2)与H2加成产物为2,3-二甲基丁烷,则该烯烃可能有2种结构 |
2.下列有关说法中正确的是( )
| A. | 100g98%的浓H2SO4中所含的氧原子数为4NA(NA为阿伏伽德罗常数,下同) | |
| B. | 3.1g白磷晶体中含有的P-P键数是0.6NA | |
| C. | 向Ca(HCO3)2溶液中加入Ca(OH)2溶液至过量:Ca2++2HCO3-+2OH-═CaCO3↓+CO${\;}_{3}^{2-}$+2H2O | |
| D. | 冰水中常会形成(H2O)x(x≥1)分子,原因是存在氢键 |
19.乙烯的相关转化关系如图.下列说法正确的是( )
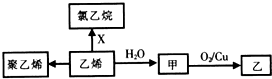

| A. | 聚乙烯是纯净物 | B. | X为C12 | ||
| C. | CH3OCH3与甲互为同分异构体 | D. | 甲→乙反应类型为取代反应 |
20.下列说法正确的是( )
| A. | 蔗糖、淀粉、油脂及其水解产物均为非电解质 | |
| B. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| C. | 用新制Cu(OH)2悬浊液可以鉴别乙酸、乙醇和葡萄糖 | |
| D. | 分子组成为CH4或C2H6O的有机物不存在同分异构现象 |