题目内容
19.乙烯的相关转化关系如图.下列说法正确的是( )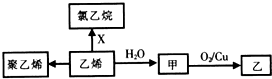
| A. | 聚乙烯是纯净物 | B. | X为C12 | ||
| C. | CH3OCH3与甲互为同分异构体 | D. | 甲→乙反应类型为取代反应 |
分析 A、乙烯发生加聚反应生成聚乙烯,聚乙烯中聚合度不同;
B、乙烯与氯化氢发生加成反应生成氯乙烷;
C、乙烯与水发生加成反应生成乙醇;
D、乙醇在铜作催化剂条件下生成乙醛.
解答 解:A、聚乙烯中由于聚合度你n不同,故聚乙烯为混合物,故A错误;
B、乙烯与氯化氢发生加成反应生成氯乙烷,故X是HCl,不是氯气,故B错误;
C、乙烯与水发生加成反应生成乙醇,乙醇的分子式为CH3CH2OH,与甲醚是同分异构体,故C正确;
D、乙醇在铜作催化剂条件下生成乙醛,此反应属于氧化反应,故D错误,
故选C.
点评 本题主要考查的是乙烯的性质,涉及反应类型的判断、试剂的选择等,难度不大.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
9.下列物质中,加入水中显著放热并且生成碱的是( )
| A. | 生石灰 | B. | 食盐 | C. | 浓硫酸 | D. | 硝酸铵 |
10.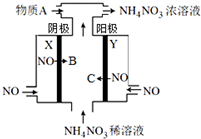 电解NO制备 NH4NO3的工作原理如图所示,X、Y皆为Pt电极,为使电解产物全部转化为NH4NO3,需补充物质A.下列说法正确的是( )
电解NO制备 NH4NO3的工作原理如图所示,X、Y皆为Pt电极,为使电解产物全部转化为NH4NO3,需补充物质A.下列说法正确的是( )
 电解NO制备 NH4NO3的工作原理如图所示,X、Y皆为Pt电极,为使电解产物全部转化为NH4NO3,需补充物质A.下列说法正确的是( )
电解NO制备 NH4NO3的工作原理如图所示,X、Y皆为Pt电极,为使电解产物全部转化为NH4NO3,需补充物质A.下列说法正确的是( )| A. | 在阴极NO转化为B,B为硝酸根离子 | |
| B. | 电解一段时间,阴极附近pH升高 | |
| C. | 为使电解产物全部转化为NH4NO3,需补充的A为硝酸 | |
| D. | 该电解池的阳极反应式为:NO-3e-+4OH-=NO${\;}_{3}^{-}$+2H2O |
7.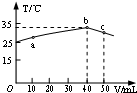 25℃时,向盛有50mL pH=2的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述不正确的是( )
25℃时,向盛有50mL pH=2的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述不正确的是( )
 25℃时,向盛有50mL pH=2的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述不正确的是( )
25℃时,向盛有50mL pH=2的HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述不正确的是( )| A. | b点时酸碱恰好完全反应 | |
| B. | a→b的过程中,混合溶液中可能存在:c(A)=c(Na+) | |
| C. | HA溶液的物质的量浓度为0.01mol•L-1 | |
| D. | 25℃时,HA的电离平衡常数K约为1.43×10-3 |
14.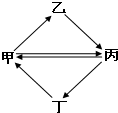 下列各组物质按如图所示转化关系每一步都能一步实现的是
下列各组物质按如图所示转化关系每一步都能一步实现的是
( )
 下列各组物质按如图所示转化关系每一步都能一步实现的是
下列各组物质按如图所示转化关系每一步都能一步实现的是| 甲 | 乙 | 丙 | 丁 | |
| A | FeCl3 | FeCl2 | Fe2O3 | Fe(OH)3 |
| B | Cu | CuO | CuSO4 | CuCl2 |
| C | C | CO | CO2 | H2CO3 |
| D | NH3 | NO | NO2 | HNO3 |
| A. | A | B. | B | C. | C | D. | D |
4.下列关于有机物莽草酸(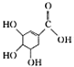 )和鞣酸(
)和鞣酸(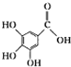 )的叙述中,正确的是( )
)的叙述中,正确的是( )
 )和鞣酸(
)和鞣酸( )的叙述中,正确的是( )
)的叙述中,正确的是( )| A. | 两种有机物中含有完全相同的官能团 | |
| B. | 两种酸都能与溴水反应,且反应类型相同 | |
| C. | 分别向两种酸中滴加三氯化铁溶液,均发生显色反应 | |
| D. | 等物质的量的两种酸与NaOH反应,消耗NaOH的量不同 |
11.金属材料的发展在人类文明发展中起着巨大的作用.下列金属中用电解方法进行冶炼的是( )
| A. | 铝 | B. | 铜 | C. | 银 | D. | 铁 |
8.短周期元素X、Y、Z、W的原子序数逐渐增大,其中X原子的电子数与电子层数相等,Z为短周期中金属性最强的元素,Y与X、Y与Z均能形成原子个数比为1:1和1:2的两种化合物,Y和W同主族.下列说法正确的是( )
| A. | Y与Z形成的两种化合物中所含化学键类型完全相同 | |
| B. | 化合物X2W比化合物X2Y稳定 | |
| C. | Y、Z、W三种元素形成的化合物的水溶液一定呈中性 | |
| D. | 原子半径:r(Z)>r(W)>r(Y)>r(X) |
7.下列有关有机反应的叙述正确的是( )
| A. | 采用分子筛固体酸作为苯和丙烯反应的催化剂来制备异丙苯,符合绿色化学工艺 | |
| B. | 一定条件下,所有的醇均能发生脱水反应形成碳碳双键或碳碳三键 | |
| C. | 石油的裂化、裂解都是化学变化,煤的气化、液化都是物理变化 | |
| D. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |