题目内容
1.下列有关物质性质比较的叙述中不正确的是( )| A. | 稳定性:溶液>胶体>浊液 | B. | 溶解性:NaHCO3>Na2CO3 | ||
| C. | 酸性:HCl>H2CO3>HClO | D. | 氧化性:浓HNO3>稀HNO3>稀HCl |
分析 A.分散质粒子直径越小越稳定;
B.常温下,向饱和碳酸钠溶液中通入二氧化碳气体,有碳酸氢钠晶体析出;
C.次氯酸是弱酸;
D.浓度越大氧化性越强.
解答 解:A.分散质粒子直径越小越稳定,稳定性:溶液>胶体>浊液,故A正确;
B.常温下,向饱和碳酸钠溶液中通入二氧化碳气体,有碳酸氢钠晶体析出,可知常温时水溶解性:Na2CO3>NaHCO3,故B错误;
C.盐酸是强酸,次氯酸是弱酸,酸性:HCl>H2CO3>HClO,故C正确;
D.浓度越大氧化性越强,硝酸有强氧化性,盐酸没有,故D正确.
故选B.
点评 本题考查元素周期律,侧重考查学生分析推断能力,难度不大,注意次氯酸是弱酸但属于强氧化性酸.

练习册系列答案
相关题目
11.下列说法不正确的是( )
| A. | 臭氧空洞、温室效应、光化学烟雾、硝酸型酸雨的形成都与氮氧化合物有关 | |
| B. | 石油裂解、煤的气化、海水制镁、纤维素制火棉等过程中都包含化学变化 | |
| C. | 低碳经济就是以低能耗、低污染、低排放为基础的经济发展模式 | |
| D. | 可用丁达尔效应鉴别氢氧化铁胶体和氯化铁溶液 |
12.下列各组物质在溶液中相互作用,能产生白色沉淀的是( )
| A. | AgNO3和HBr | B. | Ca(HCO3)2和HNO3 | C. | Ba(NO3)2和CO2 | D. | NaHCO3和Ca(OH)2 |
16.下列有关热化学方程式书写及对应表述均正确的是( )
| A. | 密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6kJ/mol | |
| B. | 稀醋酸与0.1 mol/LNaOH溶液反应:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol | |
| C. | 已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式:2H2O(l)═2H2(g)+O2(g)△H=+285.5kJ/mol | |
| D. | 已知2C(s)+O2 (g)═2CO(g)△H=-221kJ/mol,则可知C的燃烧热△H=-110.5kJ/mol |
6.下列说法正确的是( )
| A. | 在乙醇分子间,既存在分子间作用力又存在氢键 | |
| B. | 带相反电荷离子之间的相互吸引称为离子键 | |
| C. | 同素异形体间的相互转化属于物理变化 | |
| D. | H2O比H2S稳定,因为水分子间有氢键 |
13.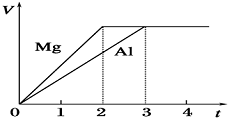 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)的关系如图所示.反应中镁和铝的( )
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)的关系如图所示.反应中镁和铝的( )
 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)的关系如图所示.反应中镁和铝的( )
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)的关系如图所示.反应中镁和铝的( )| A. | 摩尔质量之比为2:3 | B. | 失去的电子数之比为8:9 | ||
| C. | 反应速率之比为2:3 | D. | 质量之比为4:3 |
10.下列物质中既能与盐酸反应,又能与NaOH溶液反应的是( )
①Na2CO3 ②Al(OH)3 ③NH4HCO3 ④Al2O3.
①Na2CO3 ②Al(OH)3 ③NH4HCO3 ④Al2O3.
| A. | ①②④ | B. | ②③④ | C. | ②④ | D. | 全部 |
16.下列化学用语表达正确的是( )
| A. | HCl的电子式为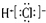 | |
| B. | S2-的结构示意图为 | |
| C. | O-16原子的符号为${\;}_{6}^{16}O$ | |
| D. | ${\;}_{12}^{6}C$、${\;}_{6}^{13}C$、${\;}_{6}^{14}C$含有相同的中子数 |