题目内容
16.下列化学用语表达正确的是( )| A. | HCl的电子式为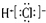 | |
| B. | S2-的结构示意图为 | |
| C. | O-16原子的符号为${\;}_{6}^{16}O$ | |
| D. | ${\;}_{12}^{6}C$、${\;}_{6}^{13}C$、${\;}_{6}^{14}C$含有相同的中子数 |
分析 A.HCl为共价化合物,电子式中不存在离子;
B.S2-的质子数为16,核外电子数为18,各层电子数分别为2、8、8,用小圈和圈内的数字表示原子核和核内质子数,弧线表示电子层,弧线上的数字表示该层的电子数;
C.质量数为16的氧原子含有8个质子、8个中子;
D.化学上常用元素符号左下角的数字表示原子的质子数,左上角的数字表示原子的中子数与质子数之和.
解答 解:A.HCl为共价化合物,组成原子最外层满足稳定结构,电子式中不存在离子,电子式为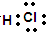 ,故A错误;
,故A错误;
B.S2-的质子数为16,核外电子数为18,各层电子数分别为2、8、8,硫离子结构示意图为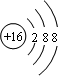 ,故B正确;
,故B正确;
C.化学上常用元素符号左下角的数字表示原子的质子数,左上角的数字表示原子的中子数与质子数之和,O-16含有8个质子、8个中子,原子的符号为816O,故C错误;
D.${\;}_{12}^{6}C$、${\;}_{6}^{13}C$、${\;}_{6}^{14}C$的中子数分别为6、7、8中子数不同,其中${\;}_{12}^{6}C$表示错误,故D错误;
故选B.
点评 本题考查了电子式、离子结构示意图、原子符号的书写判断,题目难度不大,注意掌握常见化学用语的概念及表示方法,明确离子化合物与共价化合物的电子式的区别,注意化学上常用元素符号左下角的数字表示原子的质子数,左上角的数字表示原子的中子数与质子数之和.

练习册系列答案
相关题目
1.下列有关物质性质比较的叙述中不正确的是( )
| A. | 稳定性:溶液>胶体>浊液 | B. | 溶解性:NaHCO3>Na2CO3 | ||
| C. | 酸性:HCl>H2CO3>HClO | D. | 氧化性:浓HNO3>稀HNO3>稀HCl |
11.运用元素周期律分析下面的推断,其中不正确的是( )
| A. | 锂(Li)与水反应比钠与水反应剧烈 | |
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 | |
| C. | 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 | |
| D. | HBrO4的酸性比HClO4弱 |
8.已知A2-、B-、C+、D2+、E3+五种简单离子的核外电子数相等,则它们对应的核电荷数由大到小的顺序是( )
| A. | A>B>C>D>E | B. | B>A>C>D>E | C. | C>D>E>A>B | D. | E>D>C>B>A |
6.下列各组物质的稀溶液相互反应,把前者逐滴滴入后者与把后者逐滴滴入前者,所产生的现象相同的是( )
| A. | AlCl3 和NaOH | B. | Na2CO3和HCl | C. | Na2CO3和H2SO4 | D. | NaCl和AgNO3 |

 Al(OH)3+OH-.
Al(OH)3+OH-.
