题目内容
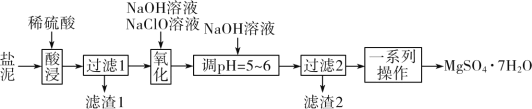
【题目】向100mLNaOH溶液中通入标况下的CO21.12L后,将溶液小心蒸干后得到不含结晶水的固体5.08g,则下列说法中正确的是 ( )
A.原NaOH溶液的浓度是1.00mol/L,所得固体是Na2CO3
B.原NaOH溶液的浓度是0.500mol/L,所得固体是Na2CO3和NaHCO3
C.原NaOH溶液的浓度是1.00mol/L,所得固体是Na2CO3和NaOH
D.原NaOH溶液的浓度是0.900mol/L,所得固体是Na2CO3和NaHCO3
【答案】D
【解析】
n(CO2)=![]() =0.05mol,假设得到的固体是Na2CO3,m(Na2CO3)=106g/mol×0.05mol=5.3g,假设得到的固体是NaHCO3,m(NaHCO3)=0.05mol×84g/mol=4.2g,实际上得到的固体介于二者之间,所以得到的固体是Na2CO3和NaHCO3的混合物,设Na2CO3和NaHCO3的物质的量分别是xmol、ymol,根据C原子守恒有x+y=0.05,根据固体质量有106x+84y=5.08,联立为方程组解得:x=0.04,y=0.01,根据Na原子守恒得n(NaOH)=2n(Na2CO3)+n(NaHCO3)=2×0.04mol+0.01mol=0.09mol,c(NaOH)=
=0.05mol,假设得到的固体是Na2CO3,m(Na2CO3)=106g/mol×0.05mol=5.3g,假设得到的固体是NaHCO3,m(NaHCO3)=0.05mol×84g/mol=4.2g,实际上得到的固体介于二者之间,所以得到的固体是Na2CO3和NaHCO3的混合物,设Na2CO3和NaHCO3的物质的量分别是xmol、ymol,根据C原子守恒有x+y=0.05,根据固体质量有106x+84y=5.08,联立为方程组解得:x=0.04,y=0.01,根据Na原子守恒得n(NaOH)=2n(Na2CO3)+n(NaHCO3)=2×0.04mol+0.01mol=0.09mol,c(NaOH)=![]() =0.9mol/L,
=0.9mol/L,
答案选D。

【题目】湿法炼锌产生的铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质,生产金属镉的工艺流程如下:
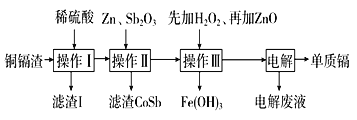
下表列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1 mol/L)
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.2 |
沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(1)酸浸时粉碎铜镉渣的目的是__________。
(2)操作Ⅰ产生的滤渣主要成分为________(填化学式)。
(3)①操作Ⅲ中先加入适量H2O2,发生反应的离子方程式为______。
②再加入ZnO控制反应液的pH,pH范围为______。
③若加入的H2O2不足,加入ZnO后所得的电解液中会含有Fe元素。请设计实验方案鉴别________。
(4)净化后的溶液用惰性电极电解可获得镉单质。电解废液中可循环利用的溶质是_________。