题目内容
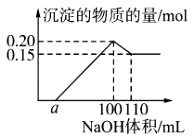
向20mL2mol/LNaAlO2溶液中,加入50mLHCl溶液,充分反应后,得0.78g沉淀,则HCl溶液的物质的量浓度为 ( )
| A.0.2mol/L | B.2.6mol/L | C.4mol/L | D.5mol/L |
AB
试题分析:偏铝酸钠的物质的量是0.04mol,而氢氧化铝的物质的量是0.01mol。因此反应中偏铝酸钠过量,或者是偏铝酸钠完全消耗,生成的氢氧化铝又部分被溶解。则根据有关的方程式NaAlO2+HCl+H2O=Al(OH)3+NaCl、Al(OH)3+3HCl=AlCl3+3H2O可知,当偏铝酸钠过量时,消耗盐酸是0.01mol,则浓度是0.2mol/L;如果盐酸过量,则消耗的盐酸是0.04mol+(0.04mol-0.01mol)×3=0.13mol,则盐酸的浓度是2.6mol/L,答案选AB。
点评:该题是高考中的常见题型,属于中等难度的试题。试题贴近高考,灵活性强。有利于考查学生分析问题、解决问题的能力。该题关键是准确判断出反应的两种情况,然后列式计算即可,否则或漏选。

练习册系列答案
相关题目
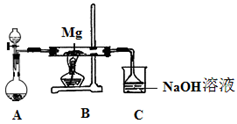
 2MgSO3+S;丙同学的推测是:3Mg+SO2
2MgSO3+S;丙同学的推测是:3Mg+SO2