题目内容
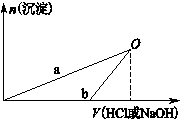
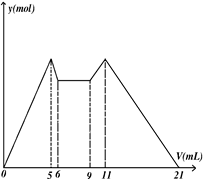
右图是向MgCl2、AlCl3混合溶液中,开始滴加7ml试剂A,之后改滴试剂B,所得沉淀ymol 与试剂体积V(ml)间的关系.以下结论不正确的是

| A.横坐标从5到6溶液中Al3+浓度在上升 |
| B.原混合液中,c(Al3+)∶c(Mg2+)∶c(Cl—)=1∶1∶5 |
| C.A是NaOH,B是盐酸,且c(NaOH)∶c(HCl)=2∶1 |
| D.横坐标从6到9,相应离子反应式H++OH— =H2O |
A
试题分析:向MgCl2、AlCl3混合溶液中,开始滴加7ml试剂A,之后改滴试剂B。
横坐标从5到6溶液中,是生成的氢氧化铝转化为偏铝酸钠的过程,所以溶液中根本就不存在Al3+,所以也就无所谓下降和上升。错误,故选A.向MgCl2、AlCl3混合溶液中,开始滴加7ml试剂A,之后改滴试剂B。可以从图像上看到,镁离子和铝离子先转化为沉淀,而后沉淀又消失,说明,A是NaOH,B是盐酸,从量的关系可以看到:从0-5沉淀达到最大值,从11-21沉淀完全消失,所以浓度存在以下关系:c(NaOH)∶c(HCl)=2∶1,所以C正确;从6-9沉淀一致不变,说明加入的盐酸是在和刚开始加入的未反应完的氢氧化钠反应,所以D正确;从0-5沉淀达到最大值,从5-6氢氧化铝转化为偏铝酸钠。消耗的氢氧化钠比例关系是5:1,生成沉淀消耗的氢氧化钠的比例关系是3:2 ,所以根据电荷守恒可得:原混合液中,c(Al3+)∶c(Mg2+)∶c(Cl—)=1∶1∶5,B正确。故选A。
点评:本题重点是要会书写,氢氧化铝能溶于强碱,对应的关系式AlCl3+3NaOH=Al(OH)3↓+H2O Al(OH)3+NaOH=NaAlO2+2H2O。

练习册系列答案
相关题目
 X溶液
X溶液 Al(OH)3沉淀
Al(OH)3沉淀 Y溶液
Y溶液 Al(OH)3沉淀
Al(OH)3沉淀