题目内容
【题目】A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,B和X均可与A形成10电子的化合物;B与Z的最外层电子数之比为2:3,化合物Y2X2与水反应生成X的单质,所得溶液可使酚酞变红。请回答下列问题。
(1)Z的原子结构示意图为_______,化合物BA4的电子式为__________。
(2)化合物Y2X2中含有的化学键类型有________________________。
(3)化合物A2X和A2Z中,沸点较高的是_________(填化学式),其主要原因是______。
(4)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为______________________________________________。
【答案】 ![]()
![]() 离子键、非极性共价键 H2O 水分子间形成氢键 H2O2 + H2S = S↓ + 2H2O
离子键、非极性共价键 H2O 水分子间形成氢键 H2O2 + H2S = S↓ + 2H2O
【解析】A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,B和X均可与A形成10电子的化合物,因此A是H,则Y是Na;B与Z的最外层电子数之比为2:3,分别位于第二周期和第三周期,则B是C,Z是S。化合物Y2X2与水反应生成X的单质,所得溶液可使酚酞变红,因此X是O,据此解答。
根据以上分析可知A是H,B是C,X是O,Y是Na,Z是S。则
(1)S的原子结构示意图为![]() ,化合物CH4是共价化合物,电子式为
,化合物CH4是共价化合物,电子式为![]() 。
。
(2)化合物Y2X2是过氧化钠,其中含有的化学键类型有离子键、非极性共价键。
(3)由于水分子间形成氢键,所以沸点较高的是H2O。
(4)A与X和A与Z均能形成18个电子的化合物,分别是双氧水和硫化氢,二者可以发生氧化还原反应,反应的化学方程式为H2O2 +H2S=S↓+2H2O。

【题目】合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:
温 度(℃) | 360 | 440 | 520 |
K值 | 0.036 | 0.010 | 0.0038 |
(1)①由上表数据可知该反应的ΔH_____ 0(填填“>”、“=”或“<”)。
②下列措施能用勒夏特列原理解释是_____(填序号)。
a.增大压强有利于合成氨 b.使用合适的催化剂有利于快速生成氨
c.生产中需要升高温度至500°C左右 d.需要使用过量的N2,提高H2转化率
(2)0.2mol NH3溶于水后再与含有0.2mol H2SO4的稀溶液完全反应放热Q kJ,请你用热化学方程式表示其反应式:___________________________________。
(3)常温时,将a mol氨气溶于水后,再通入b mol氯化氢,溶液体积为1L,且c(NH4+)=c(Cl﹣),则一水合氨的电离平衡常数Kb=_____(用ab表示)。
(4)原料气H2可通过反应 CH4(g)+H2O (g)![]() CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的
CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的![]() 恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
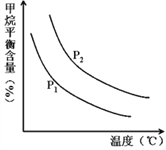
①图中,两条曲线表示压强的关系是:P1_____P2(填“>”、“=”或“<”)。
②其它条件一定,升高温度,氢气的产率会______(填“增大”,“减小”减小,“不变”不变)。
(5)原料气H2还可通过反应CO(g)+H2O(g)![]() CO2(g)+H2(g)获取。
CO2(g)+H2(g)获取。
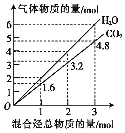
①T℃时,向容积固定为5 L的容器中充入1mol H2O(g)和1mol CO, 反应达平衡后,测得CO的浓度0.08 mol/L,该温度下反应的平衡常数K值为_____。
②保持温度仍为T℃,容积体积为5L,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是_____(填序号)。
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6