题目内容
【题目】下表是周期表中的一部分,根据A~J在周期表中的位置,用元素符号或化学式回答下列问题:
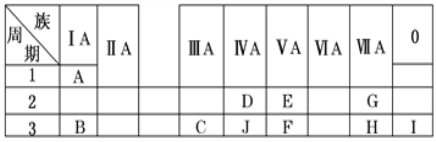
(1)表中元素,化学性质最不活泼的是________,只有负价而无正价的元素是________。(填元素符号)
(2)最高价氧化物的水化物中酸性最强的是________,呈两性的是________。
(3)在B、C、E、F中,原子半径最大的是________。
(4)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:________。
(5)与C元素同族的第5周期元素X的价电子排布式________________。
【答案】 Ar F HClO4 Al(OH)3 Na Al(OH)3+NaOH===NaAlO2+2H2O 5s25p1
【解析】根据元素在周期表中的相对位置,首先判断出元素,然后结合元素周期律和相关物质的性质解答。
根据A~J在周期表中的位置可知A是H,B是Na,C是Al,D是C,E是N,F是P,G是F,H是Cl,I是Ar,J是Si。则
(1)表中元素,化学性质最不活泼的是稀有气体元素Ar。F是最活泼的非金属,只有负价而无正价的元素是F。
(2)非金属性越强,最高价含氧酸的酸性越强,F没有含氧酸,则最高价氧化物的水化物中酸性最强的是HClO4,呈两性的是Al(OH)3。
(3)同周期自左向右原子半径逐渐减小,同主族从上到下原子半径逐渐增大,因此在B、C、E、F中,原子半径最大的是Na。
(4)氢氧化铝是两性氢氧化物,与氢氧化钠溶液反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O。
(5)与Al元素同族的第5周期元素X是In,其价电子排布式为5s25p1。

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案【题目】通常人们把拆开1 mol某化学键吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估计化学反应的反应热。下列是一些化学键的键能。
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol | 414 | 489 | 565 | 155 |
根据键能数据估算反应CH4+4F2=CF4+4HF每消耗1mol CH4的热效应( )
A. 放热1940 kJ B. 吸热1940 kJ C. 放热485 kJ D. 吸热485 kJ