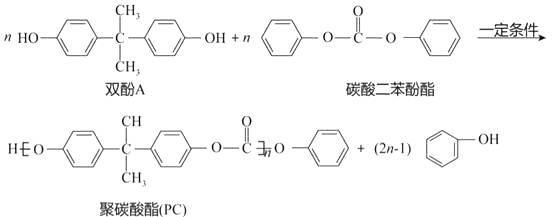
题目内容
【题目】通常人们把拆开1 mol某化学键吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估计化学反应的反应热。下列是一些化学键的键能。
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol | 414 | 489 | 565 | 155 |
根据键能数据估算反应CH4+4F2=CF4+4HF每消耗1mol CH4的热效应( )
A. 放热1940 kJ B. 吸热1940 kJ C. 放热485 kJ D. 吸热485 kJ
【答案】A
【解析】根据ΔH=反应物的化学键断裂吸收的能量-生成物的化学键形成释放的能量解答。
根据键能数据可知反应CH4+4F2=CF4+4HF的ΔH=(4×414+4×155-4×489-4×565)kJ·mol![]() =-1940 kJ·mol
=-1940 kJ·mol![]() ,因此每消耗1molCH4的热效应为放热1940 kJ。
,因此每消耗1molCH4的热效应为放热1940 kJ。
答案选A。

练习册系列答案
相关题目