题目内容
【题目】加热N2O5时,发生以下两个分解反应:N2O5N2O3+O2 , N2O3N2O+O2 , 在1L密闭容器中加热 4mol N2O5达到化学平衡时c(O2)为4.50mol/L,c(N2O3)为1.62mol/L,则在该温度下各物质的平衡浓度正确的是( )
A.c(N2O5)=1.44 mol/L
B.c(N2O5)=0.94 mol/L
C.c(N2O)=1.40 mol/L
D.c(N2O)=3.48 mol/L
【答案】B
【解析】解:加热N2O5时,发生以下两个分解反应:N2O5N2O3+O2,N2O3N2O+O2,则
N2O5 | N2O3+ | O2 | N2O3 | N2O+ | O2 | ||
起始 | 4 | 0 | 0 | x | 0 | x | |
转化 | x | x | x | y | y | y | |
平衡 | 4﹣x | x | x | x﹣y | y | x+y | |
化学平衡时c(O2)为4.50mol/L,c(N2O3)为1.62mol/L,
则 ![]() ,解得x=3.06,y=1.44,
,解得x=3.06,y=1.44,
c(N2O5)=4﹣3.06=0.94mol/L,c(N2O)=1.44mol/L,
故选B.
【考点精析】利用化学平衡的计算对题目进行判断即可得到答案,需要熟知反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.

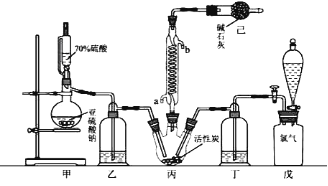
【题目】某化学兴趣小组利用如图装置制取氨气并探究氨气的有关性质。

(1)装置A中烧瓶内试剂可选用___________(填序号)。
a.碱石灰 b.浓硫酸 c.生石灰 d.五氧化二磷 e.烧碱固体
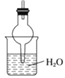
(2)若探究氨气的溶解性,需在K2的导管末端连接下表装置中的______(填序号)装置,当装置D中集满氨气后,关闭K1、K2,打开K3,引发喷泉的实验操作是________。
备选装置(其中水中含酚酞溶液) | ||
|
|
|
Ⅰ | Ⅱ | Ⅲ |
(3)若探究氨气的还原性,需打开K1、K3,K,2处导管连接制取纯净、干燥氯气的装置。
①用二氧化锰与浓盐酸制取氯气生成气体必须通过盛有_________试剂的洗气瓶;
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为_________。
③从K3处导管逸出的气体中含有少量C12,则C装置中应盛放______溶液(填化学式),反应的离子方程式为_____。