题目内容
【题目】用A+、B-、C2-、D、E、F分别表示含有18个电子的几种微粒(离子或分子),请回答下列问题:
(1)A元素是________、B元素是________、C元素是________(用元素符号表示)。
(2)B的单质可用来制“84”消毒液的主要成分,写出反应的离子方程式_____________。
(3)用文字描述比较B、C两元素的非金属性强弱的方法(必要时可用方程式,至少一条):________________。
(4)D是由两种元素组成的双原子分子,用电子式表示其形成过程___________________。
(5)E是所有含18个电子的微粒中氧化能力最强的分子,其与水反应的化学方程式为________。
(6)F分子中含有4个原子,既有极性键又有非极性键,其电子式是_____________。
【答案】 K Cl S Cl2+2OH-=Cl-+ClO-+H2O Cl2+S2-=2Cl-+S或Cl2+H2S=2HCl+S ![]() 2F2+2H2O=4HF+O2
2F2+2H2O=4HF+O2 ![]()
【解析】A+、B-、C2-、D、E、F分别表示含有18个电子的几种微粒(离子或分子),因此A是K,B是Cl,C是S,D、E、F可能是H2O2、H2S、HCl、F2、Ar等,据此解答。
(1)根据以上分析可知A元素是K、B元素是Cl、C元素是S。
(2)B的单质氯气可用来制“84”消毒液的主要成分,该反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O。
(3)氯气能把硫化钠氧化为单质硫,可以说明氯元素非金属性强于硫元素,反应的离子方程式为Cl2+S2-=2Cl-+S。
(4)D是由两种元素组成的双原子分子,因此D是HCl,含有共价键的共价化合物,用电子式表示其形成过程为![]() 。
。
(5)E是所有含18个电子的微粒中氧化能力最强的分子,E是单质氟,其与水反应的化学方程式为2F2+2H2O=4HF+O2。
(6)F分子中含有4个原子,既有极性键又有非极性键,F是双氧水,含有共价键的共价化合物,其电子式是![]() 。
。

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案【题目】Sn 元素位于元素周期表第IVA 族,SnCl4可用作媒染剂和催化剂,工业上常用氯气与金属锡在300℃反应制备SnCl4。SnCl4 极易水解,SnCl2、SnCl4的一些物理数据如下:
物质 | 状态 | 熔点/℃ | 沸点/℃ |
Sn | 银白色固体 | 232 | 2260 |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
用下列装置合成四氯化锡(夹持装置略)。注:在仪器3 中各加入0.6 mL浓硫酸,实验操作如下:
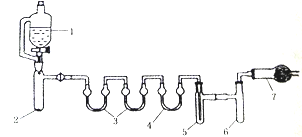
I.把干燥的仪器按图示装置连接好,在仪器1中加入B mL浓盐酸,在仪器2中加入2.0g KMnO4,在仪器5中加入2~3颗Sn粒;
II.打开活塞,让盐酸流下,均匀产生Cl2并充满整套装置,然后加热Sn粒,将生成的SnCl4收集在仪器6中;
III.Sn粒反应完毕后,停止加热,同时停止滴加盐酸,取下仪器6,迅速盖好盖子。
请回答:
(1)写出仪券2中发生化学反应方程式________________________。
(2)下列说法不正确的是______。
A.装置连接好,加入药品前要检查装置的气密性
B.产生的Cl2先充满整套装置,这步操作不可以省略
C.操作中应控制盐酸的滴入速率,不能太快,也不能太慢
D.仪器6 可用冰水浴冷却,也可以自然冷却
(3)仪器7 放的试剂是_______________________,作用是___________________、__________________。
(4)SnCl4在空气中与水蒸气反应除生成白色SnO2·xH2O固体,还可以看到___________________现象,化学方程式为___________________________________。
(5)经测定产品中含有少量的SnCl2,可能的原因___________( 用化学方程式表示)。
(6)产品中含少量SnCl2,测定SnCl4纯度的方法:取0.400 g产品溶于50 mL的稀盐酸中,加入淀粉溶液作指示剂,用0.0100mol/L碘酸钾标准溶液滴定至终点,消耗标准液8.00 mL,反应原理为:3SnCl2+ KIO3+ 6HCl==3SnCl4+ KI+ 3H2O,判断滴定终点的依据为______________________________,产品的纯 度为___________________________________。
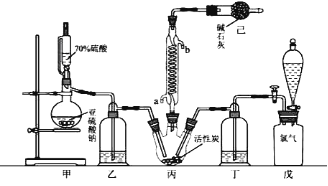
【题目】某化学兴趣小组利用如图装置制取氨气并探究氨气的有关性质。

(1)装置A中烧瓶内试剂可选用___________(填序号)。
a.碱石灰 b.浓硫酸 c.生石灰 d.五氧化二磷 e.烧碱固体
(2)若探究氨气的溶解性,需在K2的导管末端连接下表装置中的______(填序号)装置,当装置D中集满氨气后,关闭K1、K2,打开K3,引发喷泉的实验操作是________。
备选装置(其中水中含酚酞溶液) | ||
|
|
|
Ⅰ | Ⅱ | Ⅲ |
(3)若探究氨气的还原性,需打开K1、K3,K,2处导管连接制取纯净、干燥氯气的装置。
①用二氧化锰与浓盐酸制取氯气生成气体必须通过盛有_________试剂的洗气瓶;
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为_________。
③从K3处导管逸出的气体中含有少量C12,则C装置中应盛放______溶液(填化学式),反应的离子方程式为_____。