题目内容
下列有关氧化还原反应的叙述中正确的是( )
| A、有单质参加或有单质生成的反应一定是氧化还原反应 |
| B、金属单质在化学反应中一定作还原剂 |
| C、失电子的反应物在反应中作氧化剂,反应中被还原 |
| D、氧化还原的本质是元素化合价的升降 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:A.有单质参加或有单质生成的反应不一定是氧化还原反应;
B.失电子的反应物作还原剂;
C.失电子的反应物作还原剂,被氧化;
D.氧化还原反应的本质是电子转移.
B.失电子的反应物作还原剂;
C.失电子的反应物作还原剂,被氧化;
D.氧化还原反应的本质是电子转移.
解答:
解:A.有单质参加或有单质生成的反应不一定是氧化还原反应,如同素异形体之间的转化,故A错误;
B.失电子的反应物作还原剂,在化学反应中,金属单质失电子作还原剂,故B正确;
C.失电子的反应物作还原剂,被氧化,得电子的物质在反应中作氧化剂,被还原,故C错误;
D.氧化还原反应的本质是电子转移,其特征是元素化合价升降,故D错误;
故选B.
B.失电子的反应物作还原剂,在化学反应中,金属单质失电子作还原剂,故B正确;
C.失电子的反应物作还原剂,被氧化,得电子的物质在反应中作氧化剂,被还原,故C错误;
D.氧化还原反应的本质是电子转移,其特征是元素化合价升降,故D错误;
故选B.
点评:本题考查了氧化还原反应,根据反应中元素化合价变化结合基本概念分析解答,注意氧化还原反应本质和特征的区别,题目难度不大.

练习册系列答案
相关题目
我国政府规定,国内销售的食盐必须加碘.关于加碘的下列叙述中不正确的是( )
| A、加碘食盐开袋后,不宜长期放置后食用 |
| B、加碘食盐中不能同时加碘化钾和碘酸钾 |
| C、加碘食盐中加入的是单质碘 |
| D、加碘食盐中加入是碘酸钾 |
反应4A(s)+3B(g)?2C(g)+D(g),经2min B的浓度减少0.6mol/L,对此反应速率的正确表示是( )
| A、在2min末,用B表示的反应速率是0.3mol/(L?min) |
| B、在2min内,用D表示的反应速率是0.1mol/(L?min) |
| C、反应速率v(B):v(C)=3:2 |
| D、在该条件下,再经2 min后,B的浓度减少0.6mol/L |
下列说法正确的是( )
| A、需要通电才可进行的有:电解、电泳、电离、电镀、电化腐蚀 |
| B、在Fe(OH)3胶体中滴加稀硫酸的现象为:先沉淀后溶解 |
| C、蛋白酶是蛋白质,它可以催化蛋白质的水解反应,还可以催化淀粉的水解反应 |
| D、在Fe(OH)3胶体中插入两电极通电,在阳极附近颜色加深 |
关于分子式为C5H10的烯烃的下列说法正确的是( )
| A、该烯烃的一种同分异构体为CH2=CHCH(CH3)2名称为2-甲基-3-丁烯 |
| B、其属于烯烃的同分异构体有5种 |
| C、有一种同分异构体的名称为:2,2-二甲基-1-丙烯 |
| D、该物质的结构简式最多有两个侧链 |
下列实验设计或实验操作中,正确的是( )
A、 铜与浓硝酸反应制取NO2 |
B、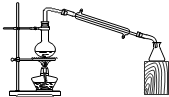 该装置设计合理,可实现石油的分馏 |
C、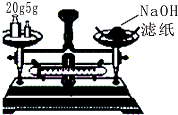 称量25g氢氧化钠 |
D、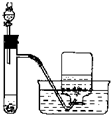 H2O2溶液与MnO2制备O2 |
下列系统命名法正确的是( )
| A、2-甲基-4-乙基戊烷 |
| B、2-甲基-3-丁炔 |
| C、2,2-二甲基-4-丁醇 |
| D、2,3-二乙基-1-戊烯 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1mol Cl2与足量的铁反应,转移的电子数为3NA |
| B、在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA |
| C、将pH=2的盐酸和pH=4的硫酸等体积混合,所得溶液pH=3 |
| D、1mol OH-和1mol-OH(羟基)中含有的质子数均为9NA |