题目内容
汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)?2ΝΟ(g)△H>0,已知该反应在2404℃时,平衡常数K=64×10-4.请回答:
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟后O2的物质的量为0.5mol,则N2的反应速率 .
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志 .
A.消耗1mol N2同时生成1mol O2 B.混合气体密度不变
C.混合气体平均相对分子质量不变 D.2v(N2)正=v(NO)逆
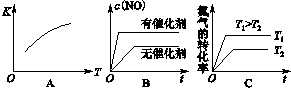
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是 (填字母序号).
(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态.与原平衡状态相比,此时平衡混合气中NO的体积分数 .(填“变大、“变小”或“不变”)
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应 (填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是 .
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟后O2的物质的量为0.5mol,则N2的反应速率
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志
A.消耗1mol N2同时生成1mol O2 B.混合气体密度不变
C.混合气体平均相对分子质量不变 D.2v(N2)正=v(NO)逆
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态.与原平衡状态相比,此时平衡混合气中NO的体积分数
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应
考点:化学平衡状态的判断,化学平衡建立的过程,化学平衡的影响因素,化学平衡的计算
专题:化学平衡专题
分析:(1)5分钟内,△n(O2)=1mol-0.5mol=0.5mol,由N2(g)+O2(g)?2NO(g)可知△n(N2)=0.5mol,带入v=
计算;
(2)可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变,以此分析;
(3)根据温度、催化剂对反应速率和平衡移动的影响判断;
(4)根据化学方程式的特点结合压强对平衡的影响分析;
(5)计算某时刻生成物的浓度幂之积与反应物浓度幂之积的比值,与该温度下的平衡常数相比较,可得出结论.
| △n |
| V?△t |
(2)可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变,以此分析;
(3)根据温度、催化剂对反应速率和平衡移动的影响判断;
(4)根据化学方程式的特点结合压强对平衡的影响分析;
(5)计算某时刻生成物的浓度幂之积与反应物浓度幂之积的比值,与该温度下的平衡常数相比较,可得出结论.
解答:
解:(1)5分钟内,△n(O2)=1mol-0.5mol=0.5mol,由N2(g)+O2(g)?2NO(g)可知△n(N2)=0.5mol,v(N2)=
=
=0.05mol/(L?min),
故答案为:0.05mol/(L?min);
(2)A.消耗1mol N2等效于消耗1mol O2,同时生成1mol O2,故选;
B.混合气体密度一直不变,故不选;
C.混合气体平均相对分子质量不变,总质量是个定值,总物质的量是个定值,混合气体的平均相对分子质量一直不变,故不选;
D.2v(N2)正=v(NO)正=v(NO)逆,故选;
故选:AD;
(3)(3)A、该反应的正反应为吸热反应,则升高温度平衡向正反应进行,平衡常数增大,故A正确;
B、加入催化剂,反应速率增大,但平衡不发生移动,故B错误;
C、升高温度,反应速率增大,平衡向正反应方向移动,氮气的转化率增大,故C正确.
故答案为:AC;
(4)该反应中,气体的化学计量数之和前后相等,压强对平衡移动没有影响,只要是在相同温度下,则平衡状态相同,与原平衡状态相比,此时平衡混合气中NO的体积分数,故答案为:不变;
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,则有该时刻生成物的浓度幂之积与反应物浓度幂之积的比值为:
=9×10-4<K,则反应应向正反应方向进行,
故答案为:向正反应方向进行 因为浓度商Qc<K.
| △n |
| V?△t |
| 0.5mol |
| 2L×5min |
故答案为:0.05mol/(L?min);
(2)A.消耗1mol N2等效于消耗1mol O2,同时生成1mol O2,故选;
B.混合气体密度一直不变,故不选;
C.混合气体平均相对分子质量不变,总质量是个定值,总物质的量是个定值,混合气体的平均相对分子质量一直不变,故不选;
D.2v(N2)正=v(NO)正=v(NO)逆,故选;
故选:AD;
(3)(3)A、该反应的正反应为吸热反应,则升高温度平衡向正反应进行,平衡常数增大,故A正确;
B、加入催化剂,反应速率增大,但平衡不发生移动,故B错误;
C、升高温度,反应速率增大,平衡向正反应方向移动,氮气的转化率增大,故C正确.
故答案为:AC;
(4)该反应中,气体的化学计量数之和前后相等,压强对平衡移动没有影响,只要是在相同温度下,则平衡状态相同,与原平衡状态相比,此时平衡混合气中NO的体积分数,故答案为:不变;
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,则有该时刻生成物的浓度幂之积与反应物浓度幂之积的比值为:
| (3×10-3 )2 |
| (2.5×10-1)×(4.0×10-2) |
故答案为:向正反应方向进行 因为浓度商Qc<K.
点评:本题考查化学平衡的有关计算,题目难度中等,注意平衡常数的计算和应用.

练习册系列答案
相关题目
下列有关氧化还原反应的叙述中正确的是( )
| A、有单质参加或有单质生成的反应一定是氧化还原反应 |
| B、金属单质在化学反应中一定作还原剂 |
| C、失电子的反应物在反应中作氧化剂,反应中被还原 |
| D、氧化还原的本质是元素化合价的升降 |
固体NH5属于离子晶体.它与水反应的化学方程式为NH5+H2O→NH3?H2O+H2↑,它也能跟乙醇发生类似的反应,并都产生氢气.下列有关NH5叙述正确的是( )
| A、含有NH4+和H- |
| B、NH5中N元素的化合价为+5价 |
| C、1mol NH5中含有5NA个N-H键 |
| D、与乙醇反应时,NH5被还原 |
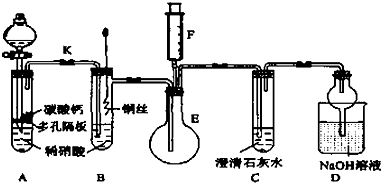
用如图所示装置进行实验,装置正确且设计合理的是( )

| A、用图①所示装置收集HCl气体 |
| B、用图②所示装置配制一定物质的量浓度的硫酸 |
| C、用图③所示装置检查该装置的气密性 |
| D、用图④所示装置进行实验室制取的实验 |
在恒温、恒容的密闭容器中进行反应A(g)?B(g)+C(g).若反应物的浓度由2mol/L降到0.8mol/L需20s,那么反应物浓度由0.8mol/L降到0.2mol/L所需反应时间为( )
| A、10s | B、大于10s |
| C、小于10s | D、无法判断 |
25℃、101kPa下:①2Na(s)+
O2(g)═Na2O(s)△H1=-414kJ?mol-1②2Na(s)+O2(g)═Na2O2(s)△H2=-511kJ?mol-1,下列说法正确的是( )
| 1 |
| 2 |
| A、①和②产物的阴阳离子个数比不相等 |
| B、①和②生成等物质的量的产物,转移电子数不同 |
| C、25℃、101kPa下,Na2O2(s)+2Na(s)═2Na2O(s)△H=-317 kJ?mol-1 |
| D、常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
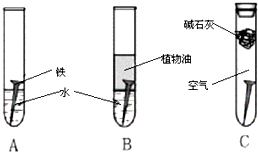 某研究小组对铁生锈进行研究:
某研究小组对铁生锈进行研究: