题目内容
【题目】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下:

根据设计要求回答:
(1)B装置有三种功能:①控制气流速度; ②均匀混合气体; ③____________。
(2)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x取值范围________。
(3)E装置的作用是________(填编号)。
A.收集气体 B.吸收氯气
C.防止倒吸 D.吸收氯化氢
(4)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式:_______________________________________。
(5)E装置中除生成盐酸外,还含有有机物,从E中分离出有机物的最佳方法为________。
该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为________(填编号)。
A CH4 B CH3Cl C CH2Cl2 D CHCl3 E CCl4
【答案】干燥混合气体 大于或等于4 CD CH4 + 2Cl2 ![]() C + 4HCl 分液 ab
C + 4HCl 分液 ab
【解析】
在加热条件下,浓盐酸和二氧化锰反应生成氯气,浓硫酸具有吸水性,可以作干燥剂,C中甲烷和氯气在光照条件下发生取代反应生成氯代烃和HCl,尾气中含有氯化氢,氯化氢能溶于水、碱性溶液,所以E装置是处理尾气,倒置的干燥管能防倒吸,据此分析解答。
(1)装置B中盛放浓硫酸,它具有吸水性,因为甲烷和氯气中含有水蒸气,所以浓硫酸可以均匀并干燥混合气体;通过观察气泡能控制气流速率,
故答案为:干燥混合气体;
(2)根据CH4与Cl2的反应可知欲获得较多的HCl,也就是使CH4中的H原子全部转化为HCl,此时消耗的Cl2的物质的量至少是CH4物质的量的4倍,即x的取值范围为:大于或等于4;
(3)E装置可吸收氯化氢,还可防止倒吸,故CD项正确,答案选CD;
(4)黑色小颗粒为C,则该反应的化学方程式为:CH4 + 2Cl2 ![]() C + 4HCl;
C + 4HCl;
(5)E装置中除了有盐酸生成外,还含有二氯甲烷、三氯甲烷和四氯化碳,二氯甲烷、三氯甲烷和四氯化碳不溶于水,能分层,可用分液分开;反应生成的二氯甲烷、三氯甲烷、四氯化碳均是油状的液体,只有一氯甲烷是气体,还可能有过量的甲烷气体,故ab正确,答案为:分液;ab。

【题目】化学反应都有能量变化,吸热或放热是化学反应中能量变化的主要形式之一。
Ⅰ.丙烷(C3H8)是一种优良的燃料,下图是一定量丙烷完全燃烧生成CO2和1molH2O(I)过程中的能量变化图。试回答下列问题:

(1)写出丙烷燃烧的热化学方程式:__________。
(2)二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1mol二甲醚完全燃烧生成CO2和液态水放出1455kJ的热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1645kJ的热量,则混合气体中丙烷和二甲醚的物质的量之比为__________。
Ⅱ.用下图所示的装置进行中和热的测定实验,分别取50mL0.55mol/L的NaOH溶液、50mL0.25mol/L的硫酸进行实验,回答下列问题:
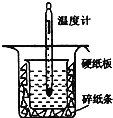
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是__________,除此之外,装置中的一个明显错误是__________。
(2)近似认为0.55mol/L的NaOH溶液和0.25mol/L的硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃),通过以下数据计算中和热△H=__________(结果保留小数点后一位)。
温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | ||
H2SO4 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 29.5 |
2 | 27.0 | 27.4 | 27.2 | 32.3 |
3 | 25.9 | 25.9 | 25.9 | 29.2 |
4 | 26.4 | 26.2 | 26.3 | 29.8 |
(3)若改用60mL0.25mol/L的H2SO4和50mL0.55mol/L的NaOH溶液进行反应,与上述实验相比,所放出的热量__________(填“相等”或“不相等”)。 所求中和热___(填“等”或“不相等”),简述理由__________________________________________。
(4)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)_____。
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.将以上四实验测量温度均纳入计算平均值