题目内容
4.(1)R2+离子核外有a个电子,b个中子,R原子表示为:a+2a+b+2R,S2-的离子结构示意图: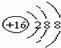 ,Br -的电子式:
,Br -的电子式: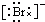 ,CO2的结构式:O=C=O
,CO2的结构式:O=C=O(2)用电子式表示下列化合物的形成过程:
CaF2:

H2O:
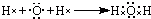 .
.
分析 (1)阳离子的质子数=核外电子数-所带电荷,质量数=质子数+质子数,元素符合左下角的数字表示质子数,左上角数字表示质量数;硫离子的核电荷数为16,核外有3个电子层,最外层有8个电子;溴离子为阴离子,需要标出所带电荷及最外层电子;二氧化碳分子中含有两个碳氧双键;
(2)氟化钙为离子化合物,阴阳离子需要标出所带电荷,氟离子需要标出最外层电子;水为共价化合物,分子中含有两个氧氢键.
解答 解:(1)R2+离子核外有a个电子,b个中子,则R原子的质子数为a+2,质量数为a+b+2,R原子符号为:a+2a+b+2R;
硫离子核外有3个电子层,最外层有8个电子,其离子结构示意图为: ;
;
溴离子的最外层达到8电子稳定结构,溴离子的电子式为: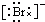 ;
;
二氧化碳为共价化合物,其分子中含有两个碳氧双键,二氧化碳的结构式为:O=C=O,
故答案为: ;a+2a+b+2R;
;a+2a+b+2R;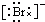 ;O=C=O;
;O=C=O;
(2)氟化钙为离子化合物,阴阳离子需要标出所带电荷,用电子式表示其形成过程为: ;
;
H2O为共价化合物,各原子达到稳定结构,用电子式表示形成过程为: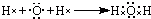 ,
,
故答案为: ;
;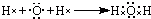 .
.
点评 本题考查了常见化学用语的书写,题目难度中等,明确电子式、离子结构示意图、元素符号、结构式等概念及书写原则为解答关键,试题知识点较多,充分考查了学生的灵活应用能力及规范答题能力.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
14.设阿伏加德罗常数为NA,下列说法正确的是( )
| A. | 0.1mol乙醇中含有C-H键的数目为0.6NA | |
| B. | 12g金刚石含有碳碳键数为4NA | |
| C. | 常温常压下,0.2mol的SiO2所含分子数为0.2NA | |
| D. | 31g白磷(P4)中含有(3/2)NA个P-P键 |
12.分子式为C5H10的烯烃,考虑顺反异构的情况下,其同分异构体的数目为( )
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
19.A、B、C、D 四种原子序数小于18 的元素,其离子 aA+、bB2+、cC-、dD2-具有相同的电子层结构,下列判断正确的是( )
| A. | 原子序数的大小顺序是:B<A<C<D | |
| B. | 离子半径由大到小的顺序是:B2+>A+>C->D2- | |
| C. | A、B、C、D四种元素原子具有相同的电子层数 | |
| D. | 金属性A>B,非金属性C>D |
9.下列说法正确的是( )
| A. | 共价键都具有方向性 | |
| B. | 键能越大表示该分子越容易受热分解 | |
| C. | 乙醇分子与水分子之间只存在范德华力 | |
| D. | 氯的各种含氧酸的酸性由强到弱排列为HClO4>HClO3>HClO2>HClO |
13.两种有机物以一定比例混合,一定条件下在a L O2(足量)中燃烧,充分反应后恢复到原状态,再通过足量Na2O2层,得到气体仍是a L,下列混合有机物中符合此条件的是( )
| A. | CH4、C2H4 | B. | CH3OH、CH3COOH | C. | C2H6、HCHO | D. | HCHO、CH3COOCH3 |
 ②HCl
②HCl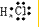 ③Cl2
③Cl2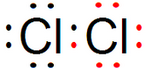 ④CO2
④CO2 ⑤KCl
⑤KCl
 ②Br2
②Br2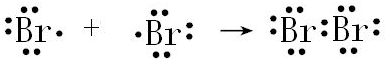 .
.