题目内容
18.在25℃时,有pH为x的盐酸和pH为y的NaOH溶液,取Vx L该盐酸同该NaOH溶液中和,需Vy L NaOH溶液.问:(1)若x+y=14,$\frac{Vx}{Vy}$=1:1(填数值);
(2)若x+y=13,$\frac{Vx}{Vy}$=1:10(填数值);
(3)若x+y>14,$\frac{Vx}{Vy}$=10x+y-14(表达式),
且Vx>Vy(填“>”、“<”或“=”)(题中x≤6,y≥8).
分析 25℃时、有pH为x的HCl溶液和pH为y的NaOH溶液,取VxL该盐酸用该NaOH溶液中和,需VyLNaOH溶液,则有VxL×10-amol/L=VyL×10b-14mol/L,即$\frac{{V}_{x}}{{V}_{y}}$=10x+y-14,以此来计算.
解答 解:25℃时、有pH为x的HCl溶液和pH为y的NaOH溶液,取VxL该盐酸用该NaOH溶液中和,需VyLNaOH溶液,则有VxL×10-xmol/L=VyL×10y-14mol/L,即$\frac{{V}_{x}}{{V}_{y}}$=10x+y-14,
①若x+y=14,则$\frac{{V}_{x}}{{V}_{y}}$=10x+y-14=1:1,故答案为:1:1;
②若x+y=13,则$\frac{{V}_{x}}{{V}_{y}}$=10x+y-14=1:10,故答案为:1:10;
③若x+y>14,则$\frac{{V}_{x}}{{V}_{y}}$=10xy-14>1,即Vx>Vy,故答案为:10x+y-14;>.
点评 本题考查盐类水解和酸碱中和的计算,明确溶液不显电性及原子守恒的关系、酸碱中和时氢离子与氢氧根离子的物质的相同是解答本题的关键,题目难度中等.

练习册系列答案
相关题目
5.某容积固定的密闭容器内发生反应X(g)+2Y(g)?2Z(g)△H=akJ•mol-1(a>0),若向密闭容器中通入1molX和2molY,达平衡状态时,吸收热量bKJ,则下列判断正确的是( )
| A. | 当a=b>0时,该反应达到化学平衡状态 | |
| B. | 该反应达到化学平衡状态时,一定有a>b | |
| C. | 当密闭容器内气体密度不再改变时,该反应达到化学平衡状态 | |
| D. | 密闭容器中X和Y的物质的量之比为1:2时,该反应达到化学平衡状态 |
6.在a-b-稀H2SO4组成的原电池装置中,a的金属性比氢强,b为碳棒,关于此装置的各种叙述不正确的是( )
| A. | 碳棒上有气体放出,溶液pH变大 | B. | a是正极,b是负极 | ||
| C. | 电子从a极流向b极 | D. | a极上发生了氧化反应 |
3.下列除去杂质所用的试剂和方法错误的是( )
| A. | 除去Na2CO3 固体中混有的少量的NaHCO3:置于坩埚中加热 | |
| B. | 除去FeCl2溶液中的FeCl3:加入铁粉 | |
| C. | 除去氢氧化铁胶体中所含的盐酸:过滤 | |
| D. | 除去CO2中混有的少量的HCl:通过饱和的NaHCO3溶液中洗气 |
10.某些建筑材料中含有氡(Rn),氡是放射性元素. 222Rn、219Rn、220Rn分别来自镭、锕、钍,因而分别称为镭射气、锕射气和钍射气.下列有关氡的说法,正确的是( )
| A. | 氡是双原子分子 | |
| B. | 氡气因其化学性质活泼而对人体有害 | |
| C. | 氡气因其具有放射性而对人体有害 | |
| D. | 222Rn、219Rn、220Rn是三种同素异形体 |
7.化合物Y2X在水中能电离出具有相同电子层结构的阴阳离子,该化合物可能为( )
| A. | H2O | B. | Na2O | C. | K2S | D. | Na2S |
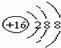 ,Br -的电子式:
,Br -的电子式: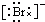 ,CO2的结构式:O=C=O
,CO2的结构式:O=C=O
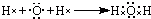 .
.