题目内容
燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等。
(1)对燃煤废气进行脱硝处理时,常利用甲烷催化还原氮氧化物:
①CH4 (g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g) ΔH=-570 kJ·mol-1
②CH4(g)+4NO(g)="=2" N2(g) +CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
则CH4 (g)+2NO2(g)="=" N2(g)+CO2(g)+2H2O(g) ΔH=___________。
(2)将燃煤废气中的CO2转化为甲醚的反应原理为:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)
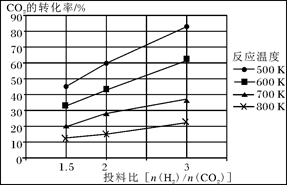
已知在压强为a MPa下,该反应在不同温度、不同投料比时,CO2的转化率见下图: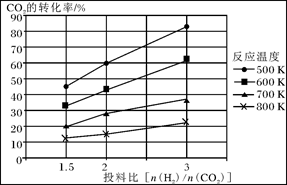
①此反应为 (填“放热”、“吸热”);若温度不变,提高投料比[n(H2)/n(CO2)],则K将________(填“增大”、“减小”或“不变”)。
②若用甲醚作为燃料电池的原料,请写出在碱性介质中电池正极的电极反应式_______________________。
③在a MPa和一定温度下,将6 mol H2和2 mol CO2在2 L密闭容器中混合,当该反应达到平衡时,测得平衡混合气中CH3OCH3的体积分数约为16.7%(即1/6),此时CO2的转化率是多少?(计算结果保留2位有效数字)
④在a MPa和500K下,将10mol H2和5 mol CO2在2 L密闭容器中混合,5min达到平衡,请在答题卡的坐标图中画出H2浓度变化图。(请标出相应的数据)

(1)对燃煤废气进行脱硝处理时,常利用甲烷催化还原氮氧化物:
①CH4 (g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g) ΔH=-570 kJ·mol-1
②CH4(g)+4NO(g)="=2" N2(g) +CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
则CH4 (g)+2NO2(g)="=" N2(g)+CO2(g)+2H2O(g) ΔH=___________。
(2)将燃煤废气中的CO2转化为甲醚的反应原理为:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)已知在压强为a MPa下,该反应在不同温度、不同投料比时,CO2的转化率见下图:

①此反应为 (填“放热”、“吸热”);若温度不变,提高投料比[n(H2)/n(CO2)],则K将________(填“增大”、“减小”或“不变”)。
②若用甲醚作为燃料电池的原料,请写出在碱性介质中电池正极的电极反应式_______________________。
③在a MPa和一定温度下,将6 mol H2和2 mol CO2在2 L密闭容器中混合,当该反应达到平衡时,测得平衡混合气中CH3OCH3的体积分数约为16.7%(即1/6),此时CO2的转化率是多少?(计算结果保留2位有效数字)
④在a MPa和500K下,将10mol H2和5 mol CO2在2 L密闭容器中混合,5min达到平衡,请在答题卡的坐标图中画出H2浓度变化图。(请标出相应的数据)
(1)-865 kJ/mol (2) ① 放热;不变; ② O2 +4e-+2H2O ==4OH-
③设平衡时CO2的转化率为x。
2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)
开始 1 3 0 0
转化 x 3x x/2 3x/2
平衡 (1-x) (3-3x) x/2 3x/2
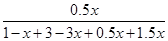 ×100%=16.7%
×100%=16.7%
解得:x=0.80即CO2的转化率为80%。
④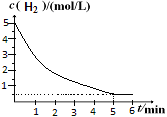
③设平衡时CO2的转化率为x。
2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)开始 1 3 0 0
转化 x 3x x/2 3x/2
平衡 (1-x) (3-3x) x/2 3x/2
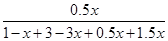 ×100%=16.7%
×100%=16.7%解得:x=0.80即CO2的转化率为80%。
④

试题分析:(1)①+②整理可得CH4 (g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH=-865 kJ/mol。(2)①由CO2的转化率图可知:升高温度,CO2的转化率降低;在相同的温度时,n(H2):n(CO2)越高,CO2的转化率越大。升高温度,CO2的转化率降低,说明升高温度,化学平衡逆向移动。根据平衡移动原理,升高温度,化学平衡向吸热反应方向移动,因此正反应为放热反应。化学平衡常数K只与温度有关,温度不变,化学平衡常数就不变。③在反应开始时c(CO2)=1mol/L,c(H2)="3mol/L;" c(CH3OCH3)="0," c(H2O)=0.假设CO2转化浓度为x,则Δc(H2)="2xmol/L;" Δc(CH3OCH3)="x/2mol/L;" Δc(H2O)= 3x/2mol/L。平衡时各种物质的浓度分别是c(CO2)="(1-x)mol/L;" c(H2)=(3-2x)mol/L; c(CH3OCH3)="x/2mol/L;" c(H2O)= 3x/2mol/L。平衡混合气中CH3OCH3的体积分数约为16.7%(即1/6)所以
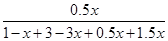 ×100%=16.7%;解得x= x=0.80即CO2的转化率为80%。④在反应开始时c(H2)=5mol/L,c(CO2)=" 2.5" mol/L; [n(H2)/n(CO2)]=2,假设反应过程中Δc(CO2)="amol/L;" Δc(H2)="3amol/L;" Δc(CH3OCH3)="a/2mol/L;" Δc(H2O)= 3a/2mol/L则当反应达到平衡时由于CO2的转化率为60%,所以
×100%=16.7%;解得x= x=0.80即CO2的转化率为80%。④在反应开始时c(H2)=5mol/L,c(CO2)=" 2.5" mol/L; [n(H2)/n(CO2)]=2,假设反应过程中Δc(CO2)="amol/L;" Δc(H2)="3amol/L;" Δc(CH3OCH3)="a/2mol/L;" Δc(H2O)= 3a/2mol/L则当反应达到平衡时由于CO2的转化率为60%,所以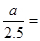 60%,所以a=1.5mol/L.因此平衡时c(H2)= (5-3a)mol/L=0.5mol/L.可画图如上述答案。略。
60%,所以a=1.5mol/L.因此平衡时c(H2)= (5-3a)mol/L=0.5mol/L.可画图如上述答案。略。
练习册系列答案
相关题目
 H2(g)+
H2(g)+  2NO2(g) ΔH 的体系中,n(NO)随时间的变化如表:
2NO2(g) ΔH 的体系中,n(NO)随时间的变化如表:
 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:

 CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。
CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。
 CH3OH(g)的平衡常数K=__________。相同温度下,若开始时加入CH3OH(g)的物质的量是原来的2倍,则__________(填序号)是原来的2倍。
CH3OH(g)的平衡常数K=__________。相同温度下,若开始时加入CH3OH(g)的物质的量是原来的2倍,则__________(填序号)是原来的2倍。 2NH3(g) △H<0。现将10 mol N2和26 mol H2置于容积可变的密闭容器中,N2的平衡转化率(
2NH3(g) △H<0。现将10 mol N2和26 mol H2置于容积可变的密闭容器中,N2的平衡转化率( )与体系总压强(P)、温度(T)的关系如图所示。回答下列问题:
)与体系总压强(P)、温度(T)的关系如图所示。回答下列问题: