题目内容
【题目】25℃时,KHS溶液里存在下列平衡:a.HS-+H2O ![]() H3O++S2- b.HS-+H2O
H3O++S2- b.HS-+H2O![]() OH-+H2S。
OH-+H2S。
(1)平衡a是_______平衡(填“电离”或“水解”,下同),平衡b是_______平衡。
(2)向KHS溶液中加入少量NaOH固体,c(S2-)将__________(填“增大”、“减小”或“不变”,下同),向KHS溶被中通入HCl时,c(HS-)将__________。
(3)向KHS溶液中加入CuSO4溶液,有黑色沉淀(CuS)产生,则平衡a__________移动(填“正向”、“逆向”或“不”,下同),平衡b__________移动。
(4)在KHS溶液中,c(OH-)-c(H+)=____________________。
(5)向KHS溶液中加入AlCl3溶液,产生的现象为______________________________。
【答案】电离 水解 增大 减小 正向 逆向 ![]() 生成白色沉淀和具有臭鸡蛋气味的气体
生成白色沉淀和具有臭鸡蛋气味的气体
【解析】
(1)根据方程式可知平衡a中生成水合氢离子,可看成是水加上氢离子;平衡b中生成氢氧根离子,据此分析判断;
(2)依据外界碱或酸对HS-的水解和电离平衡产生的影响作答;
(3)铜离子与硫离子反应会生成黑色的CuS沉淀,据此分析作答;
(4)根据质子守恒规律得出结论;
(5)Al3+与HS-发生双水解。
(1)根据方程式可知平衡a中生成氢离子,是电离平衡,平衡b中生成H2S,是水解平衡,
故答案为:电离;水解;
(2)向KHS溶液中加入氢氧化钠固体时生成硫离子,则c(S2-)将增大,向KHS溶液中通入HCl时生成H2S,则c(HS-)将减小;
故答案为:增大;减小;
(3)向KHS溶液中加入硫酸铜溶液时,有黑色沉淀(CuS)产生,说明平衡向电离的方向进行,则平衡a正向移动,促进电离,平衡b逆向移动,
故答案为:正向;逆向;
(4)在KHS溶液中,遵循质子守恒规律,即![]() ,所以
,所以![]() ,
,
故答案为:![]() ;
;
(5)向KHS溶液中加入AlCl3溶液,发生双水解反应,其离子方程式为:![]() ,所以现象为:生成白色沉淀和具有臭鸡蛋气味的气体,
,所以现象为:生成白色沉淀和具有臭鸡蛋气味的气体,
故答案为:生成白色沉淀和具有臭鸡蛋气味的气体。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】足量锌与一定量浓H2SO4充分在加热下反应生成会SO2和H2的混合气体。现有甲乙两研究小组分别实验探究:
(1)甲研究小组按下图实验验证锌与浓硫酸反应生成物中含有SO2和H2。取一定量的Zn置于b中,向a中加入100mL 18mol·L-1的浓硫酸,经过一段时间,恰好完全反应。
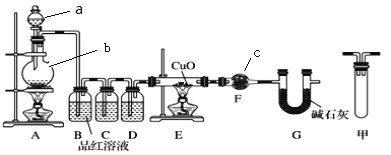
①填写仪器名称:c___________。
②实验开始前应先检验装置的气密性,请回答如何检验装置A的气密性___________。
③用化学方程式表示产生SO2的原因______________。
④U型管G的作用为__________。
⑤有同学认为A、B间应增加图中的甲装置,该装置的作用为__________。
⑥实验结束后测得装置F增重18.0g,计算实验开始时加入的Zn的质量为________g。你认为实际消耗Zn的质量应比计算值____________。(填“大”、“小”或“相同”)
(2)乙研究小组为了探究锌与稀硫酸反应过程中的速率及能量的变化,进行以下实验,分析影响反应速率的因素。
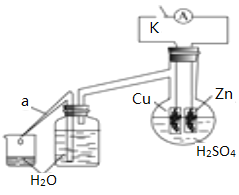
实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1分钟内从a管流出的水滴数,得到的水滴数如下表所示:
1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
分析反应过程中的水滴数,请回答:
由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率快,主要原因是________。