题目内容
3.写出甲苯与高锰酸钾反应的化学方程式5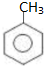 +6KMnO4+9H2SO4→
+6KMnO4+9H2SO4→ +3K2SO4+6MnSO4+14H2O.
+3K2SO4+6MnSO4+14H2O.
分析 甲苯被酸性高锰酸钾溶液氧化生成苯甲酸,同时该反应还生成硫酸钾、硫酸锰和水,据此书写方程式.
解答 解:甲苯被酸性高锰酸钾溶液氧化生成苯甲酸,同时该反应还生成硫酸钾、硫酸锰和水,反应方程式为5 +6KMnO4+9H2SO4→
+6KMnO4+9H2SO4→ +3K2SO4+6MnSO4+14H2O,
+3K2SO4+6MnSO4+14H2O,
故答案为:5 +6KMnO4+9H2SO4→
+6KMnO4+9H2SO4→ +3K2SO4+6MnSO4+14H2O.
+3K2SO4+6MnSO4+14H2O.
点评 本题考查化学反应方程式的书写,为高频考点,连接苯环的碳原子上含有H原子的苯的同系物都能被酸性高锰酸钾溶液氧化生成苯甲酸,题目难度不大.

练习册系列答案
相关题目
8.关于下列图示的说法中正确的是( )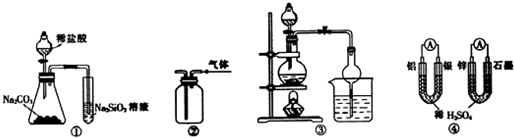

| A. | 用图①所示实验可比较氯、碳、硅三种元素的非金属性强弱 | |
| B. | 用图②所示实验装置通过排空气法收集C2H4气体 | |
| C. | 图③所示装置可用于制取乙酸乙酯,分液漏斗中装的是乙醇 | |
| D. | 图④两个装置红中能够通过导线的电子数相同时,生成的H2的物质的量也相同 |
12.湿法冶金中,把质量为m g的铁片放入CuSO4溶液中,过一会儿取出干燥,铁片的质量变为n g,则被氧化的铁的质量是( )
| A. | 8(n-m)g | B. | 8(m-n)g | C. | 7(m-n)g | D. | 7(n-m)g |
20.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,4.4g CO2与N2O混合气体中含有的原子总数为0.3NA | |
| B. | 标准状况下,2.24L乙酸中含有分子的数目为0.1NA | |
| C. | 1L 1mol•L-1的FeCl3溶液中含有Fe3+的数目为NA | |
| D. | 标准状况下,2.24 L C12与足量稀NaOH反应转移电子数为0.2NA |
 钇钡铜氧的晶胞结构如图.研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价.根据图示晶胞结构,推算晶体中Y、Ba、Cu和O原子个数比,确定其化学式为YBa2Cu3O7.
钇钡铜氧的晶胞结构如图.研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价.根据图示晶胞结构,推算晶体中Y、Ba、Cu和O原子个数比,确定其化学式为YBa2Cu3O7.