题目内容
12.关于强、弱电解质的叙述不正确的是( )| A. | 强电解质在溶液中完全电离,其水溶液中不存在分子 | |
| B. | 同一弱电解质溶液,温度不同时,导电能力不同 | |
| C. | 强电解质溶液导电能力不一定比弱电解质溶液的导电能力强 | |
| D. | 强电解质在液态时不一定会导电,但在固态时一定不导电 |
分析 A、强电解质本身能完全电离,但其溶液中存在水分子;
B、弱电解质存在电离平衡,电离过程是吸热过程,温度改变,电离平衡移动,离子浓度不同;
C、溶液导电能力取决于溶液中离子浓度的大小,与电解质强弱无关;
D、强电解质包括强酸、强碱和绝大多数盐.
解答 解:A、强电解质本身能完全电离,但其溶液中存在水分子,故水溶液中仍存在分子,故A错误;
B、弱电解质存在电离平衡,电离过程是吸热过程,温度改变,电离平衡移动,离子浓度不同,导电能力不同,故B正确;
C、溶液导电能力取决于溶液中离子浓度的大小,与离子浓度成正比,与电解质强弱无关,如果弱电解质溶液中离子浓度大于强电解质溶液,则弱电解质溶液导电能力大于强电解质,所以强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强,故C正确;
D、强电解质包括强酸、强碱和绝大多数盐,在液态时酸不导电,但碱和盐能导电;而无论是强酸、强碱还是盐,在固态时均不导电,故D正确.
故选A.
点评 本题考查了电解质强弱的本质区别,注意导电能力取决于溶液中离子浓度的大小,掌握概念实质是关键,题目较简单.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
2. CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标.
CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标.
(1)250℃时,以镍合金为催化剂,向4L容器中通入6mol CO2、6mol CH4,发生如下反应:
CO2(g)+CH4(g)?2CO(g)+2H2(g).平衡体系中各组分体积分数如下表:
①t min内CO2的平均反应速率为$\frac{1}{t}$mol•L-1•min-1.此温度下该反应的平衡常数K=64
②已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-802.3kJ•mol-1
CO(g)+H2O (g)=CO2(g)+H2 (g)△H=-41.2kJ•mol-1
2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ•mol-1
反应CO2(g)+CH4(g)?2CO(g)+2H2(g) 的△H=+247.3kJ•mol-1
(2)以二氧化钛表面覆盖Cu2Al2O4(难溶于水)为催化剂,可以将CO2和CH4直接氧化成乙酸.
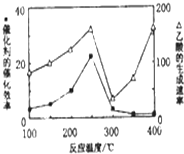
①不同温度下催化剂的催化效率与乙酸的生成速率如图所示.250~300℃时,温度升高而乙酸的生成速率降低的原因温度超过250℃时,催化剂的催化效率降低.
②为了提高该反应中CH4的转化率,可以采取的措施是增大反应压强或增大CO2的浓度等.(答一条即可)
③将Cu2Al2O4溶解在稀硝酸中的离子方程式为3 Cu2Al2O4+32 H++2 NO3-=6 Cu2++6 Al3++2 NO↑+16 H2O.
 CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标.
CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标.(1)250℃时,以镍合金为催化剂,向4L容器中通入6mol CO2、6mol CH4,发生如下反应:
CO2(g)+CH4(g)?2CO(g)+2H2(g).平衡体系中各组分体积分数如下表:
| 物质 | CH4 | CO2 | CO | H2 |
| 体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
②已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-802.3kJ•mol-1
CO(g)+H2O (g)=CO2(g)+H2 (g)△H=-41.2kJ•mol-1
2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ•mol-1
反应CO2(g)+CH4(g)?2CO(g)+2H2(g) 的△H=+247.3kJ•mol-1
(2)以二氧化钛表面覆盖Cu2Al2O4(难溶于水)为催化剂,可以将CO2和CH4直接氧化成乙酸.
①不同温度下催化剂的催化效率与乙酸的生成速率如图所示.250~300℃时,温度升高而乙酸的生成速率降低的原因温度超过250℃时,催化剂的催化效率降低.
②为了提高该反应中CH4的转化率,可以采取的措施是增大反应压强或增大CO2的浓度等.(答一条即可)
③将Cu2Al2O4溶解在稀硝酸中的离子方程式为3 Cu2Al2O4+32 H++2 NO3-=6 Cu2++6 Al3++2 NO↑+16 H2O.
3.高温、催化剂条件下,某反应达到平衡,平衡常数K=$\frac{c(CO).c({H}_{2}O)}{c(C{O}_{2}).c({H}_{2})}$.恒容时,温度升高,H2浓度减小.下列说法正确的是( )
| A. | 该反应的焓变为负值 | |
| B. | 2CO2(g)+2H2(g)?2CO(g)+2H2O(g)的平衡常数K1=K2 | |
| C. | 升高温度,正反应速率增大,逆反应速率减小,平衡正向移动 | |
| D. | 若恒容、恒温下充入CO,则K值变大 |
20.下列碱性透明溶液中,能大量共存的离子组是( )
| A. | K+、Na+、MnO${\;}_{4}^{-}$、Cl- | B. | K+、Ag+、NO${\;}_{3}^{-}$、Cl- | ||
| C. | Ba2+、Na+、Cl-、SO${\;}_{4}^{2-}$ | D. | Na+、Cu2+、NO${\;}_{3}^{-}$、Cl- |
7.实验室中,要使明矾溶液中的Al3+全部沉淀出 来,适宜用的试剂是( )
| A. | NaOH溶液 | B. | 氨水 | C. | 盐酸 | D. | Ba(OH)2溶液 |
17.如图所示,实验操作能达到相应的实验目的是( )
| A. | 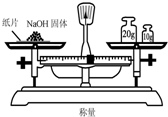 称量氢氧化钠固体的质量 称量氢氧化钠固体的质量 | |
| B. |  分离沸点相差较大的互溶液体混合物 分离沸点相差较大的互溶液体混合物 | |
| C. | 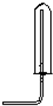 用排气法收集氯气 用排气法收集氯气 | |
| D. | 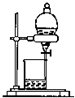 分离互不相溶的两种液体 分离互不相溶的两种液体 |
4.科学家发现了利用泪液来检测糖尿病的方法,其原理是用氯金酸钠(NaAuCl4)溶液与溶液中的葡萄糖发生反应生成纳米金单质颖粒(直径为20-60nm).下列有关说法错误的是( )
| A. | 氯金酸钠中金元素的化合价为+3 | |
| B. | 葡萄糖具有还原性 | |
| C. | 检测时,NaAuCl4发生氧化反应 | |
| D. | 纳米金单质颗粒分散在水中所得的分散系能产生丁达尔效应 |
1.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 标准状况下,2.24L CCl4所含的原子数为0.5 NA | |
| B. | 0.5 mol O2含氧原子数为0.5NA | |
| C. | 2.4 g金属镁变为镁离子时失去的电子数为0.1NA | |
| D. | 氧气和臭氧的混合物16 g中约含有NA个氧原子 |
2.在甲、乙两烧杯溶液中,分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-六种离子中的三种,已知甲烧杯的溶液呈蓝色,则乙烧杯的溶液中大量存在的离子是( )
| A. | K+、OH-、CO32 | B. | CO32-、OH-、Cl- | C. | K+、H+、Cl- | D. | Cu2+、H+、Cl- |