题目内容
6.下列物质只含有离子键的是( )| A. | CO2 | B. | CaCl2 | C. | NH4Cl | D. | NaOH |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,碱金属元素、第IIA族元素和第VIA族、第VIIA族元素之间易形成离子键,铵根离子和酸根离子之间存在离子键.
解答 解:A.二氧化碳分子中C-O原子之间只存在共价键,故A错误;
B.氯化钙中钙离子和氯离子之间只存在离子键,故B正确;
C.氯化铵中铵根离子和氯离子之间存在离子键、铵根离子中N-H原子之间存在共价键,故C错误;
D.NaOH中钠离子和氢氧根离子之间存在离子键、O-H原子之间存在共价键,故D错误;
故选B.
点评 本题考查离子键和共价键,侧重考查基本概念,明确物质构成微粒及微粒之间作用力即可解答,注意离子键和共价键的区别,题目难度不大.

练习册系列答案
相关题目
16.(1)海洋资源的开发与利用具有广阔的前景.海水的pH一般在7.5-8.6之间.某地海水中主要离子的含量如表:
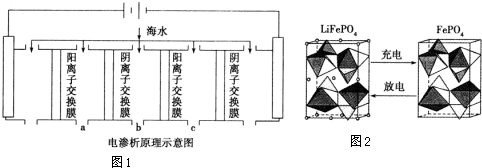
电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如图1所示.其中阴(阳)离子交换膜只允许阴(阳)离子通过.
①阴极的电极反应式为2H2O+2e-=H2↑+2OH-或2H++2e-=H2↑.
②电解一段时间,阴极区会产生水垢,其成分为CaCO3和Mg(OH)2,写出生成CaCO3的离子方程式Ca2++OH-+HCO3-=CaCO3↓+H2O.
③淡水的出口为a、b、c中的b出口.
(2)锂是制造化学电源的重要原料,如LiFePO4电池某电极的工作原理如图2所示:
该电池电解质为传导Li+的固体材料.放电时该电极是电池的正极(填“正”或“负”),电极反应式为FePO4+e-+Li+=LiFePO4.
(3)目前的研究表明,铁的某些含氧酸盐可用于工业废水、废气的处理.
①用K2FeO4处理中性废水时,K2FeO4与水反应生成氢氧化铁胶体,并放出无色无味的气体和其它物质,写出反应的离子反应方程式4FeO42-+10H2O=4Fe(OH)3(胶体)+8OH-+3O2↑,处理废水时既利用K2FeO4强氧化性,又利用生成氢氧化铁胶体的聚沉 作用.
②MFe2O4可以与氢气反应制备新型纳米材料氧缺位铁酸盐MFe2Ox(3<x<4),其中M表示+2价的金属元素,常温下,MFe2Ox能使工业废气中的SO2转化为S,达到回收硫、净化空气目的,转化过程表示如下:MFe2Ox$→_{SO_{2}}^{常温下}$MFe2Oy 则可以判断x<y,氧化性:MFe2Oy< SO2(填“>”、“<”或“=”)
| 成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | SO42- | HCO3- |
| 含量/mg•L-1 | 9360 | 83 | 200 | 1100 | 16000 | 1200 | 118 |

电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如图1所示.其中阴(阳)离子交换膜只允许阴(阳)离子通过.
①阴极的电极反应式为2H2O+2e-=H2↑+2OH-或2H++2e-=H2↑.
②电解一段时间,阴极区会产生水垢,其成分为CaCO3和Mg(OH)2,写出生成CaCO3的离子方程式Ca2++OH-+HCO3-=CaCO3↓+H2O.
③淡水的出口为a、b、c中的b出口.
(2)锂是制造化学电源的重要原料,如LiFePO4电池某电极的工作原理如图2所示:
该电池电解质为传导Li+的固体材料.放电时该电极是电池的正极(填“正”或“负”),电极反应式为FePO4+e-+Li+=LiFePO4.
(3)目前的研究表明,铁的某些含氧酸盐可用于工业废水、废气的处理.
①用K2FeO4处理中性废水时,K2FeO4与水反应生成氢氧化铁胶体,并放出无色无味的气体和其它物质,写出反应的离子反应方程式4FeO42-+10H2O=4Fe(OH)3(胶体)+8OH-+3O2↑,处理废水时既利用K2FeO4强氧化性,又利用生成氢氧化铁胶体的聚沉 作用.
②MFe2O4可以与氢气反应制备新型纳米材料氧缺位铁酸盐MFe2Ox(3<x<4),其中M表示+2价的金属元素,常温下,MFe2Ox能使工业废气中的SO2转化为S,达到回收硫、净化空气目的,转化过程表示如下:MFe2Ox$→_{SO_{2}}^{常温下}$MFe2Oy 则可以判断x<y,氧化性:MFe2Oy< SO2(填“>”、“<”或“=”)
14.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1 mol/L BaCl2溶液中含有的钡离子数为NA | |
| B. | 1 mol镁原子中含有的电子数为2NA | |
| C. | 常温常压下,11.2 L H2中含有的氢分子数为0.5NA | |
| D. | 16 g O3中含有的氧原子数为NA |
1.下列有关说法正确的是( )
| A. | 漂白粉久置于空气中会增加漂白效果 | |
| B. | 以海水为原料能制取Na、HCl、Mg、Br2等物质 | |
| C. | 蓝铜矿[Cu3(OH)2(CO3)2]也可表示为3CuO•2CO2•2H2O | |
| D. | 二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
11.将下列固体投入适量水中,再滴加酚酞,溶液不会变为红色的是( )
| A. | Na | B. | Na2O | C. | Na2CO3 | D. | NaCl |
16.室温下,下列溶液中的粒子浓度关系正确的是( )
| A. | pH=4的NaHSO3溶液中:c(Na+ )>c(HSO3-)>c(H2SO3)>c(SO32-) | |
| B. | 0.01mol•L-1 的NaHCO3 溶液中存在如下平衡:HCO3-?H++CO3 2-,加水稀释溶液中的HCO3-、H+、CO3 2-浓度减少 | |
| C. | 浓度均为0.1mol•L-1 的CH3COOH、CH3COOK混合溶液中,2c(H+)+c(CH3COOH)=2c(OH-)+c(CH3COO-) | |
| D. | 若Ka(HA)=3.6×10-4,Ka(HB)=1.75×10-5,则等物质的量浓度的NaA、KB溶液相比:c(Na+ )-c(A-)=c(K+ )-c(B-) |