题目内容
20.SO2和NOx都是大气污染物.(1)汽车排放的尾气中含CO和NO,汽车发动机工作时产生的NO和CO可通过催化转化器转化为两种无污染的气体,该反应的化学方程式是2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2.
(2)采取还原法,用炭粉可将氮氧化物还原.
已知:N2(g)+O2(g)=2NO(g)△H=+180.6kJ•mol-1
C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-1
则反应C(s)+2NO(g)=CO2(g)+N2(g)△H=-574.1kJ•mol-1.
(3)将NO2变成无害的N2要找到适合的物质G与适当的反应条件,G应为还原剂(填写“氧化剂”或“还原剂”).下式中X必须为无污染的物质,系数n可以为0.
NO2+G$\stackrel{催化剂}{→}$N2+H2O+nX (未配平的反应式).
下列化合物中,满足上述反应式中的G是ad(填写字母).
a.NH3 b.CO2 c.SO2 d.CH3CH2OH
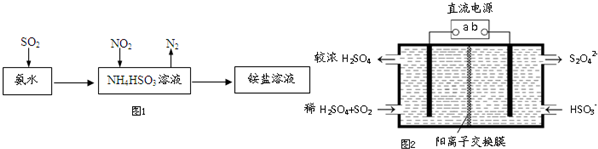
(4)利用氨水可以将SO2和NO2吸收,原理如图1所示:NO2被吸收的离子方程式是2NO2+4HSO3-=N2+4SO42-+4H+.
(5)利用图2所示装置(电极均为惰性电极)也可吸收SO2,并用阴极排出的溶液吸收NO2.
①b极的电极反应式为2HSO3-+2H++2e-=S2O42-+2H2O.
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32-生成.该反应离子方程式为4S2O42-+2NO2+8OH-═8SO42-+N2+4H2O.
分析 (1)依据CO和NO2通过催化转化器将其转化为无污染的两种气体是氮气和二氧化碳进行解答;
(2)根据盖斯定律,一个反应无论是一步完成还是分为几步完成,其热效应是相同的,据此分析;
(3)根据氧化还原反应中氧化剂和还原剂的特点结合常见的氧化剂和还原剂来回答;
(4)根据图示可知,二氧化硫溶于氨水后得到的HSO3-与二氧化氮发生氧化还原反应,据此写出离子方程式;
(5)①b极上HSO3-得电子生成S2O42-;
②依据在碱性条件下,阴极排出的溶液为S2O42-,二氧化氮与其发生反应生成氮气.
解答 解:(1)CO和NO2通过催化转化器将其转化为无污染的两种气体是氮气和二氧化碳,反应为2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2,
故答案为:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2;
(2)根据盖斯定律,一个反应无论是一步完成还是分为几步完成,其热效应是相同的,已知:
N2(g)+O2(g)=2NO(g)△H=+180.6kJ•mol-1 ①
C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-1 ②
将②-①可得:C(s)+2NO(g)=CO2(g)+N2(g)△H=-393.5kJ•mol-1-180.6kJ•mol-1=-574.1KJ/mol,故答案为:-574.1;
(3)将NO2变成无害的N2中,氮元素的化合价降低了,二氧化氮做氧化剂,需要加入还原剂,在下列四种物质:a.NH3 b.CO2 c.SO2 d.CH3CH2OH中,能被二氧化氮氧化具有还原性的物质有乙醇和NH3,故答案为:还原剂;ad;
(4)氨水可以将SO2和NO2同时吸收处理,二氧化硫与氨水反应生成亚硫酸氢根离子,NO2被吸收的离子方程式是2NO2+4HSO3-=N2+4SO42-+4H+,
故答案为:2NO2+4HSO3-=N2+4SO42-+4H+.
(5)①依据图示可知,阴极上HSO3-得电子生成S2O42-,阴极区发生反应2HSO3-+2H++2e-=S2O42-+2H2O;
故答案为:2HSO3-+2H++2e-=S2O42-+2H2O;
②阴极排出的溶液为S2O42-,二氧化氮与其发生反应,S2O42-中硫元素由+3价,变为硫酸根中硫元素为+4价,S2O42-被氧化是还原剂;二氧化氮中的氮元素化合价为+4价变为氮气0价,二氧化氮被还原为氧化剂,依据原子守恒和得失电子守恒可得,发生的离子方程式为4S2O42-+2NO2+8OH-═8SO42-+N2+4H2O,
故答案为:4S2O42-+2NO2+8OH-═8SO42-+N2+4H2O;
点评 本题考查盖斯定律的应用、氧化还原反应反应的分析以及电解原理的分析应用等,比较综合,题目难度中等,侧重于考查学生的分析能力和对基础知识的综合应用能力.

| A. | 参加反应的物质的性质是决定化学反应速率的主要因素 | |
| B. | 光是影响某些化学反应速率的外界条件之一 | |
| C. | 在给定条件下,当一个可逆反应达到平衡状态时,这就是这个反应所能达到的限度 | |
| D. | 不管什么反应,增大浓度,或加热或加压,或使用催化剂,都可以加快反应速率 |
| A. | 浊液中存在沉淀溶解平衡:AgCl (s)?Ag+(aq)+Cl-(aq) | |
| B. | 实验可以证明NH3结合Ag+能力比Cl-强 | |
| C. | 由资料信息可推知:加浓硝酸后生成的沉淀为AgCl | |
| D. | 实验表明实验室可用氨水洗涤银镜反应后的试管 |
| A. | 用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+═I2+2H2O | |
| B. | 某溶液中存在大量Fe3+、S2-、Cl-、Na+,加入NaOH溶液发生反应:Fe3++3OH-=Fe(OH)3↓ | |
| C. | 向AlCl3溶液中投入过量的Na:Na+Al3++2H2O=Na++AlO2-+2H2↑ | |
| D. | 将Na2O2固体投入H218O中:2H218O+2Na2O2=4OH-+4Na++18O2↑ |
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10 m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 | |
| 主要化合价 | 最高价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低价 | -2 | -3 | -1 | -3 | |||||
| A. | ③的熔点低于⑥的熔点 | |
| B. | 元素①与元素⑥形成的化合物皆为碱性氧化物 | |
| C. | 最高价氧化物对应水化物的酸性:⑤>⑦>④ | |
| D. | 元素④形成的氯化物中所有原子周围都达到8电子稳定结构 |
| A. | C4H10的二氯取代物有4种 | |
| B. | 最简式为C2H5的烃结构简式有5种 | |
| C. | 乙苯的一氯取代物只有3种 | |
| D. | 分子式为C4H10O且与钠反应的有机物有4种 |
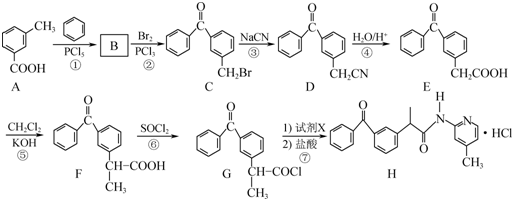
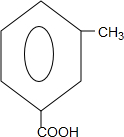 +
+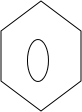 $\stackrel{PCl_{3}}{→}$
$\stackrel{PCl_{3}}{→}$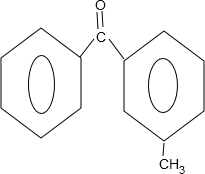 +H2O.
+H2O.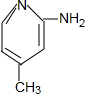 .
.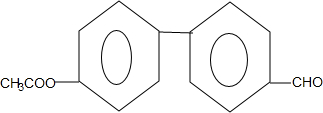 (只写一种).
(只写一种).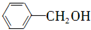 和
和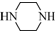 为原料制备
为原料制备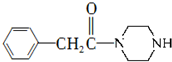 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).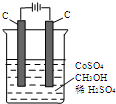 电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+).现用如图装置模拟上述过程,则:
电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+).现用如图装置模拟上述过程,则: