题目内容
1.短周期主族元素X、Y、Z、W原子序数依次增大.已知:X、Z同主族,X、Y、Z三种元素原子的最外层电子数之和为15,Y原子最外层电子数等于X原子最外层电子数的一半.下列叙述正确的是( )| A. | 原子半径:X<W<Y<Z | |
| B. | X的氢化物稳定性大于Z的氢化物稳定性 | |
| C. | X在自然界中只能以化合态形式存在 | |
| D. | W的单质可使干燥的红色布条褪色 |
分析 X、Z同主族,Y原子最外层电子数等于X原子最外层电子数的一半,令Y的最外层电子数为x,X、Z原子最外层电子式为2x,三种元素原子的最外层电子数之和为15,则x+2x+2x=15,解得x=3,短周期元素X、Y、Z、W原子序数依次递增,则X为O元素,Y为Al元素,Z为S元素,W为Cl元素,据此解答.
解答 解:X、Z同主族,Y原子最外层电子数等于X原子最外层电子数的一半,令Y的最外层电子数为x,X、Z原子最外层电子式为2x,三种元素原子的最外层电子数之和为15,则x+2x+2x=15,解得x=3,短周期元素X、Y、Z、W原子序数依次递增,则X为O元素,Y为Al元素,Z为S元素,W为Cl元素,
A.同一周期从左到右半径在减小,电子层越多原子半径越大,故原子半径为O<Cl<S<Al,故A错误;
B.X、Z同主族,自上而下金属性增强,非金属性减弱,所以非金属性X>Z,故B正确;
C.空气中含有大量的氧气,故C错误;
D.干燥的氯气没有漂白性,故D错误,
故选B.
点评 本题考查结构性质位置关系综合应用,侧重对元素周期律的考查,关键是计算确定元素种类,注意对元素周期律的理解掌握.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目
11.下列各组有机物,无论以何种物质的量的比例混合,只要总物质的量一定,则完全燃烧消耗氧气的量及生成水的量均为一恒定值的是( )
| A. | CH4和C2H4O2 | B. | C2H6O和C2H4 | C. | C3H6和C4H6 | D. | C2H2和C6H6 |
13.苯环结构中不存在C-C单键和C=C双键的交替结构,可以作为证据的事实( )
①苯不能使酸性KMnO4溶液褪色;
②苯环中碳碳键的键长均相等;
③苯能在催化剂存在和加热的条件下氢化生成环己烷;
④邻二甲苯只有一种结构;
⑤苯在FeBr3存在下同液溴发生取代反应,但不因化学反应而使溴水褪色.
①苯不能使酸性KMnO4溶液褪色;
②苯环中碳碳键的键长均相等;
③苯能在催化剂存在和加热的条件下氢化生成环己烷;
④邻二甲苯只有一种结构;
⑤苯在FeBr3存在下同液溴发生取代反应,但不因化学反应而使溴水褪色.
| A. | ②③④⑤ | B. | ①③④⑤ | C. | ①②④⑤ | D. | ①②③④ |
10.某学生为了完成一个家庭小实验,自制烷烃的分子模型,对于CnH2n+2的烷烃,做球棍模型时,除需做3n+2个球外还需要的棍(共价键)数为( )
| A. | 3n+2 | B. | 3n+1 | C. | 3n | D. | 3n-1 |
18.下列溶液一定呈中性的是( )
| A. | pH=7的溶液 | |
| B. | c(H+)=c(OH-)的溶液 | |
| C. | 由强酸、强碱等物质的量反应得到的溶液 | |
| D. | 盐溶于水得到的溶液 |
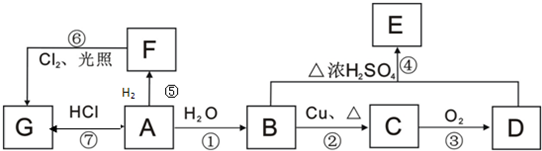
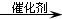
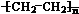 .A和水在一定条件下反应生成B,B为生活中常见的有机物,B可与另一种生活中常见有机物在一定条件下反应生成有香味的物质C,写出生成C的化学方程式
.A和水在一定条件下反应生成B,B为生活中常见的有机物,B可与另一种生活中常见有机物在一定条件下反应生成有香味的物质C,写出生成C的化学方程式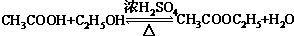 .比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射氯乙烷(沸点12.27℃)进行局部冷冻麻醉应急处理.乙烯和氯化氢在一定条件下制得氯乙烷的化学反应方程式是(有机物用结构简式表示)CH2=CH2+HC1
.比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射氯乙烷(沸点12.27℃)进行局部冷冻麻醉应急处理.乙烯和氯化氢在一定条件下制得氯乙烷的化学反应方程式是(有机物用结构简式表示)CH2=CH2+HC1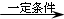 CH3CH2C1,该反应类型是加成反应.
CH3CH2C1,该反应类型是加成反应.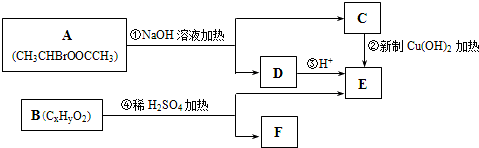
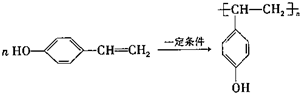 .
.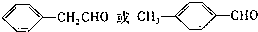 等.
等.