题目内容
15.按要求填空:(1)用系统法命名:
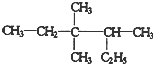 3,3,4-三甲基已烷
3,3,4-三甲基已烷(2)一定条件下某烃与H2按物质的量之比1:2加成生成 C2H5CH(CH3)2,则该烃的结构简式可能为:
 、
、 .
.(3)某具有对称结构的有机物的键线式为
 ,则其分子式为C10H16,该烃的一溴取代物有2种.
,则其分子式为C10H16,该烃的一溴取代物有2种.(4)某有机物X分子中只含C、H、O三种元素,相对分子质量小于110,其中氧元素的质量分数为14.8%,已知该物质可与FeCl3溶液发生显色反应,则X的分子式为C7H8O,若1mol X与浓溴水反应时消耗了3mol Br2,则X的结构简式为
 .
.(5)已知烯烃通过臭氧氧化并经锌和水处理得到醛或酮.例如:
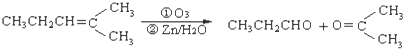 上述反应可用来推断烃分子中碳碳双键的位置.某烃A的分子式为C6H10,经过上述转化生成
上述反应可用来推断烃分子中碳碳双键的位置.某烃A的分子式为C6H10,经过上述转化生成 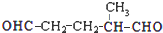 ,则烃A的结构可表示为
,则烃A的结构可表示为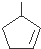 .
.
分析 (1) 为烷烃,主链为己烷,在3号C含有两个甲基,在4号C含有1个甲基,据此写出其名称;
为烷烃,主链为己烷,在3号C含有两个甲基,在4号C含有1个甲基,据此写出其名称;
(2)某烃与H2按物质的量之比1:2加成,则该烃中含有碳碳三键或两个碳碳双键,据此写出该烃可能的结构简式;
(3)根据键线式 写出其分子式;该有机物具有对称结构,其分子中含有2种等效H,所以其一溴代物有2种;
写出其分子式;该有机物具有对称结构,其分子中含有2种等效H,所以其一溴代物有2种;
(4)根据氧元素含量确定该有机物相对分子量,再根据该有机物的化学性质判断判断其分子式;再根据“1mol X与浓溴水反应时消耗了3molBr2”判断取代基位置,然后写出可能结构简式;
(5)在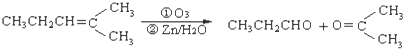 反应中,碳碳双键断裂,然后分别连接O形成醛基或羰基,据此并结合生成物
反应中,碳碳双键断裂,然后分别连接O形成醛基或羰基,据此并结合生成物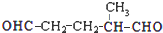 判断A的结构简式.
判断A的结构简式.
解答 解:(1) 的最长碳链含有6个C,主链为己烷,在3、3、4号C含有1个甲基,其名称为:3,3,4-三甲基已烷,
的最长碳链含有6个C,主链为己烷,在3、3、4号C含有1个甲基,其名称为:3,3,4-三甲基已烷,
故答案为:3,3,4-三甲基已烷;
(2)一定条件下某烃与H2按物质的量之比1:2加成生成C2H5CH(CH3)2,则该烃含2个双键或1个三键,则可能的结构简式为: 或
或 ,
,
故答案为: 或
或 ;
;
(3) 的分子中含有10个C、16个H原子,其分子式为:C10H16;由于该分子具有对称结构,则其分子中只有2种等效H原子,所以其一溴代物只有2种,
的分子中含有10个C、16个H原子,其分子式为:C10H16;由于该分子具有对称结构,则其分子中只有2种等效H原子,所以其一溴代物只有2种,
故答案为:C10H16,2;
(4)可与FeCl3溶液发生显色反应,则说明含有酚羟基,又X相对分子质量小于110,氧元素的质量分数为14.8%,当含有1个O原子时,其相对分子量为:$\frac{16}{14.8%}$=108,含有2个O原子时,少量为216>110,则该有机物分子中只有1个羟基,苯酚的式量为:94,该有机物式量为108,108-94=12,与苯酚相差14,即相差一个CH2,则该有机物的分子式为:C7H8O;
若1 mol X与浓溴水反应时消耗了3 mol Br2,说明酚羟基的邻位没有取代基,则甲基在羟基的间位,该有机物的结构简式为: ,
,
故答案为:C7H8O; ;
;
(5)反应产物为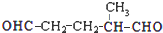 ,只有一种物质,说明反应物具有环状结构,结合已知反应原理,A分子中碳碳双键断裂,然后分别连接O原子形成
,只有一种物质,说明反应物具有环状结构,结合已知反应原理,A分子中碳碳双键断裂,然后分别连接O原子形成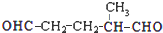 ,所以将
,所以将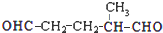 中两个碳氧双键中的O去掉,然后将碳碳双键连接即可得到A的结构简式:
中两个碳氧双键中的O去掉,然后将碳碳双键连接即可得到A的结构简式: ,
,
故答案为: .
.
点评 本题考查了有机物结构与性质,题目难度中等,涉及有机物分子式、结构简式的确定、有机物命名、加成反应原理及其应用等知识,试题知识点较多、题量较大,充分考查了学生的分析、理解能力及灵活应用基础知识都能能力.

 名校课堂系列答案
名校课堂系列答案| A. | 良好的导电性 | B. | 良好的延展性 | C. | 反应中易失电子 | D. | 良好的导热性 |
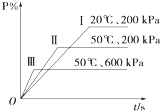 在一密闭容器中进行以下可逆反应:M(g)+P(g)═N(g)+2L.在不同的条件下P的百分含量P%的变化情况如图,则该反应( )
在一密闭容器中进行以下可逆反应:M(g)+P(g)═N(g)+2L.在不同的条件下P的百分含量P%的变化情况如图,则该反应( )| A. | 正反应放热,L是固体 | B. | 正反应吸热,L是气体 | ||
| C. | 正反应吸热,L是固态 | D. | 正反应放热,L是固体或气体 |
| A. | 氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物 | |
| B. | 碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子间的作用力 | |
| C. | 有机化合物CH3-CH2-NO2和H2N-CH2-COOH是同分异构体 | |
| D. | 加热铝使之熔化克服的是共价键 |
| A. | 5.4KJ | B. | 350KJ | C. | 3.5KJ | D. | 8.5KJ |
| A. | 适当降低温度 | B. | 将锌粒改为锌粉 | ||
| C. | 将所用硫酸换成98%的浓硫酸 | D. | 加入少量醋酸钠固体 |
| A. | 只有4种 | B. | 只有3种 | C. | 只有2种 | D. | 只有1种 |
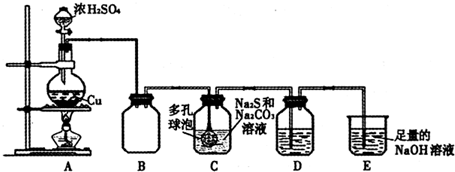
 ,它极易溶于水,是因为它与水分子间容易形成氢键,它与W元素的氢化物反应形成的化合物属于离子晶体;
,它极易溶于水,是因为它与水分子间容易形成氢键,它与W元素的氢化物反应形成的化合物属于离子晶体;