题目内容
4.实验室用3.0mol•L-1的硫酸溶液与锌粒反应制取氢气.下列措施中可能加大反应速率的是( )| A. | 适当降低温度 | B. | 将锌粒改为锌粉 | ||
| C. | 将所用硫酸换成98%的浓硫酸 | D. | 加入少量醋酸钠固体 |
分析 增大锌粒与稀硫酸的反应速率,可从影响反应速率的外界因素思考,可增大浓度、升高温度、增大固体的表面积以及形成原电池反应等,以此解答该题.
解答 解:A.降低温度,单位体积内的活化分子数减少,则反应速率减小,故A错误;
B.用锌粉代替锌粒,固体表面积增大,接触面积增大,则反应速率增大,故B正确;
C.改用98%的浓硫酸,与锌反应生成二氧化硫而不生成氢气,故C错误;
D.向该硫酸溶液中加少量醋酸钠固体,生成弱酸醋酸,溶液氢离子浓度降低,反应速率减小,故D错误.
故选B.
点评 本题考查化学反应速率的影响因素,为高频考点,把握温度、浓度、接触面积、原电池对反应速率的影响为解答的关键,注意浓硫酸的性质,题目难度不大.

练习册系列答案
相关题目
14.下列说法正确的是( )
| A. | 天然气、液化石油气、沼气的主要成分均为甲烷 | |
| B. | 煤中含有苯、甲苯及多种化工原料,可通过煤的干馏获得 | |
| C. | 石油主要是各种烷烃、环烷烃、烯烃组成的混合物 | |
| D. | 乙烯和氯乙烯都可以通过聚合反应得到高分子材料 |
12.下列各组中的微粒均含有配位键的是( )
| A. | H2O、Al2Cl6 | B. | CO2、SO42- | ||
| C. | PCl5、[Co(NH3)4Cl2]Cl | D. | NH4Cl、[Cu(NH3)4]SO4 |
19.用乙炔为原料制取CH2BrCHBrCl,可行的反应途径是在一定条件下( )
| A. | 先与Cl2加成,再与Br2加成 | B. | 先与Cl2加成,再与HBr加成 | ||
| C. | 先与HCl加成,再与Br2加成 | D. | 先与HCl加成,再与HBr加成 |
9.以下物质属于弱电解质的是( )
| A. | 盐酸 | B. | CH3COONH4 | C. | CH3COOH | D. | CI2 |
16.下列关于浓硫酸和浓硝酸的说法正确的是( )
| A. | 浓硫酸和浓硝酸都能用来直接跟锌粒反应制氢气 | |
| B. | 浓硫酸和浓硝酸都能与单质碳反应 | |
| C. | 浓硫酸和浓硝酸加水稀释后都能与金属铜反应 | |
| D. | 浓硫酸和浓硝酸在常温下都能用金属铝制容器盛放 |
13.下列有关实验的说法中,正确的是( )
| A. | 可用溴的四氯化碳溶液区分直馏汽油和裂化汽油 | |
| B. | 用NaOH、AgNO3两种溶液即可验证溴乙烷中溴元素的存在 | |
| C. | 将铜丝在酒精灯火焰上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 | |
| D. | 蛋白质溶液中分别加入浓HNO3、10%NaOH溶液、0.1%茚三酮溶液均产生白色沉淀 |
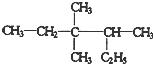 3,3,4-三甲基已烷
3,3,4-三甲基已烷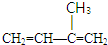 、
、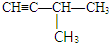 .
.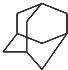 ,则其分子式为C10H16,该烃的一溴取代物有2种.
,则其分子式为C10H16,该烃的一溴取代物有2种.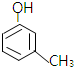 .
.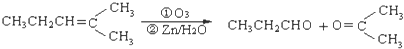 上述反应可用来推断烃分子中碳碳双键的位置.某烃A的分子式为C6H10,经过上述转化生成
上述反应可用来推断烃分子中碳碳双键的位置.某烃A的分子式为C6H10,经过上述转化生成 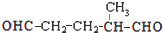 ,则烃A的结构可表示为
,则烃A的结构可表示为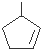 .
.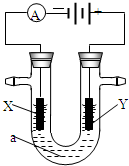 如图表示一个电解池,a是饱和NaCl溶液;X、Y都是石墨电极,U形管内滴入了几滴酚酞试液.请回答以下问题:
如图表示一个电解池,a是饱和NaCl溶液;X、Y都是石墨电极,U形管内滴入了几滴酚酞试液.请回答以下问题: