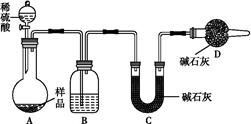
题目内容
将含有O2和CH4的混合气体置于盛有23.4 g Na2O2的密闭容器中,用电火花点燃,反应结束后,容器内的压强为零(150℃),将残留物溶于水中,无气体生成。下列叙述中正确的是( )
①混合气体中O2和CH4的体积比为2:1
②残留物只有Na2CO3
③混合气体中O2与CH4的物质的量之比为1:2
④残留物只有Na2CO3和NaOH
①混合气体中O2和CH4的体积比为2:1
②残留物只有Na2CO3
③混合气体中O2与CH4的物质的量之比为1:2
④残留物只有Na2CO3和NaOH
| A.①② | B.②③ | C.③④ | D.①④ |
C
CH4+2O2 CO2+2H2O……①;2Na2O2+2CO2=2Na2CO3+O2……②;2Na2O2+2H2O=4NaOH+O2↑……③。最后容器内压强为零,残留物溶于水无气体生成,说明反应后没有Na2O2和任何气体剩余,可以写出一个总反应方程式:①×2+②+③×2:2CH4+O2+6Na2O2=2Na2CO3+8NaOH,故③④正确。
CO2+2H2O……①;2Na2O2+2CO2=2Na2CO3+O2……②;2Na2O2+2H2O=4NaOH+O2↑……③。最后容器内压强为零,残留物溶于水无气体生成,说明反应后没有Na2O2和任何气体剩余,可以写出一个总反应方程式:①×2+②+③×2:2CH4+O2+6Na2O2=2Na2CO3+8NaOH,故③④正确。
 CO2+2H2O……①;2Na2O2+2CO2=2Na2CO3+O2……②;2Na2O2+2H2O=4NaOH+O2↑……③。最后容器内压强为零,残留物溶于水无气体生成,说明反应后没有Na2O2和任何气体剩余,可以写出一个总反应方程式:①×2+②+③×2:2CH4+O2+6Na2O2=2Na2CO3+8NaOH,故③④正确。
CO2+2H2O……①;2Na2O2+2CO2=2Na2CO3+O2……②;2Na2O2+2H2O=4NaOH+O2↑……③。最后容器内压强为零,残留物溶于水无气体生成,说明反应后没有Na2O2和任何气体剩余,可以写出一个总反应方程式:①×2+②+③×2:2CH4+O2+6Na2O2=2Na2CO3+8NaOH,故③④正确。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

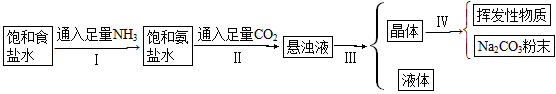
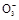
 BaCO3↓+H2O)
BaCO3↓+H2O)