题目内容
苏打和小苏打有着广泛的应用。试从反应物用量角度说明在下列用途中选A(苏打)还是B(小苏打),并说明原因。
(1)做面条时防止面粉较长时间储存变酸味,常加入适量的面碱,选用______,因为______________________________
(2)作为泡沫灭火器的药品,选用________,因为________________________
(3)用于洗涤餐具及实验室的玻璃仪器等,选用________,因为_____________
(4)治疗胃酸过多时,选用________,因为_______________________________
(提示:二者水溶液均显碱性,且苏打的碱性强)
(1)做面条时防止面粉较长时间储存变酸味,常加入适量的面碱,选用______,因为______________________________
(2)作为泡沫灭火器的药品,选用________,因为________________________
(3)用于洗涤餐具及实验室的玻璃仪器等,选用________,因为_____________
(4)治疗胃酸过多时,选用________,因为_______________________________
(提示:二者水溶液均显碱性,且苏打的碱性强)
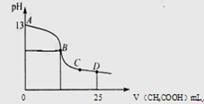
(1)A 中和等量的H+,Na2CO3比NaHCO3的用量少(质量比为53∶84)
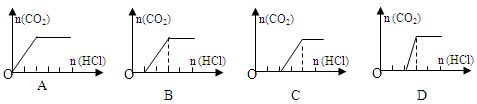
(2)B 产生等量的CO2时,NaHCO3比Na2CO3的用量少(质量比为84∶106),且产生CO2的速率快
(3)A Na2CO3碱性强,洗涤效果好
(4)B 要适量中和部分胃酸,若用苏打,碱性太强,腐蚀性强,不利于人体的健康
(2)B 产生等量的CO2时,NaHCO3比Na2CO3的用量少(质量比为84∶106),且产生CO2的速率快
(3)A Na2CO3碱性强,洗涤效果好
(4)B 要适量中和部分胃酸,若用苏打,碱性太强,腐蚀性强,不利于人体的健康
由两者的性质可知:Na2CO3+2HCl=2NaCl+H2O+CO2↑,NaHCO3+HCl=NaCl+H2O+CO2↑,中和等量酸时消耗苏打的质量相对小;产生等量CO2时消耗小苏打少;而作洗涤剂和中和胃酸时均利用其碱性,苏打碱性强,洗涤效果好,但碱性太强,不利于健康,故治疗胃酸过多应使用小苏打。

练习册系列答案
相关题目