题目内容
5.下列物质在一定条件下反应,可制得纯净1,2-二溴乙烷的是( )| A. | 乙烯与溴化氢混合 | B. | 将乙烯通入溴的四氯化碳溶液中 | ||
| C. | 乙烷与溴蒸气混合 | D. | 将乙炔通入溴的四氯化碳溶液中 |
分析 先判断该反应发生的是何种类型的反应,并分析是否有副产物生成,如果没有副产物生成则就能制取较纯净的物质.
解答 解:A、乙烯与溴化氢混合发生加成生成1-溴乙烷,不是1,2-二溴乙烷,故A错误;
B、乙烯和单质溴发生加成只生成1,2-二溴乙烷,故B正确;
C、乙烷和溴蒸气发生取代反应除了生成1,2-二溴乙烷外,还有溴化氢和其它溴代烃生成,故C错误;
D、乙炔和单质溴发生加成生成1,2-二溴乙烯,还有1,1,2,2-四溴乙烷,故D错误;
故选B.
点评 本题以物质制取为背景,考查了烃的性质,难度不大,根据反应后除了生成1,2-二氯乙烷是否还有其它物质来解答.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
16.下列装置或操作不能达到实验目的是( )
| A. | 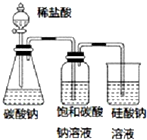 图中的实验现象能证明非金属性:Cl>C>Si | |
| B. |  图可用于实验室制备并收集乙酸乙酯 | |
| C. | 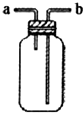 图中,气体从a口进入时,可用于收集H2、CH4、NH3等气体 | |
| D. | 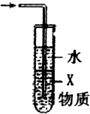 图中X若为CCl4,可用于吸收NH3或HCl |
20.NA表示阿伏加德罗常数.下列说法中正确的是( )
| A. | Cu和足量的稀硝酸反应产生4.48L气体时,转移的电子数为0.6NA | |
| B. | S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA | |
| C. | 标准状况下,44.8 L NO与22.4 LO2混合后气体中分子总数为2NA | |
| D. | 1.2g NaHSO4晶体中阳离子和阴离子的总数为0.03 NA |
10.下列说法正确的是( )
| A. | 等质量的N2和C2H4体积一定相等 | |
| B. | 凡是能发生银镜反应的物质都属于醛类 | |
| C. | 苯酚有一定毒性,不能用作消毒剂和防腐剂 | |
| D. | 溴乙烷与NaOH乙醇溶液共热生成乙烯 |
2.下列离子方程式中,正确的是( )
| A. | 氧化亚铁和稀硝酸反应FeO+2H+═Fe2++H2O | |
| B. | 硫酸铝溶液与足量烧碱:Al3++3OH-=Al(OH)3↓ | |
| C. | 氯化亚铁溶液中滴入氯水Cl2+2Fe2+═2Cl-+2Fe3+ | |
| D. | 金属铝投入NaOH溶液中2Al+2OH-+2H2O═2AlO${\;}_{2}^{-}$+2H2↑ |
 亚硝酸(HN02)在工业上用于有机合成,既具有氧化性又具有还原性,而且氧化性比还原性突出得多.回答下列问题:
亚硝酸(HN02)在工业上用于有机合成,既具有氧化性又具有还原性,而且氧化性比还原性突出得多.回答下列问题: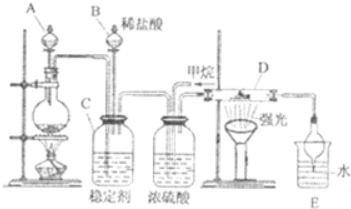 氯及其化合物在合成消毒剂、药物等方面具有广泛用途.二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,某兴趣小组通过如图装置,对二氧化氯及氯气的性质进行了研究:
氯及其化合物在合成消毒剂、药物等方面具有广泛用途.二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,某兴趣小组通过如图装置,对二氧化氯及氯气的性质进行了研究: