��Ŀ����
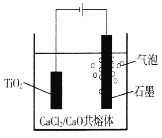
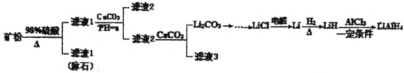
����Ŀ��������ﮣ�LiAlH4�������л��ϳɵ���Ҫ��ԭ�����Ի�﮿���Ҫ�ɷ�Li2OAl2O34SiO2��������Fe2O3��Ϊԭ�Ϻϳ�������﮵�������ͼ��
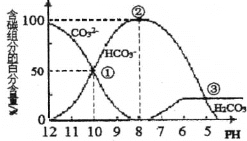
��֪���ټ��ֽ����������������pH�����ʾ��
���� | Fe(OH)3 | A1(OH)3 |
��ʼ������pH | 2.3 | 4.0 |
��ȫ������pH | 3.7 | 6.5 |
�ڳ����£�Ksp(Li2CO3)=2.0��10-3��Li2CO3��ˮ���ܽ�������¶����߶���С��
�ش��������⣺
��1�����������У��������������ʵĴ�ʩ��____ (д����)������CaCO3��������____����a������СֵΪ____��
��2������ˮϴ��Li2CO3���壬��������ˮϴ�ӣ���Ŀ����___������̼����Ƿ�ϴ����ʵ�������___��
��3��д��LiH��AlCl3��Ӧ�Ļ�ѧ����ʽ��___(��������Ҫ��)
��4����Ƽ�����Li2CO3�Ʊ���ˮLiCl��___��
��5�����л��ϳ��У���ԭ���Ļ�ԭ����ͨ��������Ч������ʾ���京����1�˻�ԭ���൱�ڶ��ٿ������Ļ�ԭ������LiAlH4������Ч��"Ϊ___��(�������2λС��)
���𰸡������ʯ�����ȡ��������Ũ�ȵ� ����pHʹAl3+��Fe3+ת������������ 6.5 ����̼��﮵���ʧ ȡ���һ��ϴ��Һ���Թ��У��μ��Ȼ�����Һ��ϡ���� AlCl3+4LiH=LiAlH4+3LiCl �������ܽ⣬���Ȼ���������������Һ 0.21
��������
��﮿�(��Ҫ�ɷ���Li2OAl2O34SiO2��������Fe2O3)Ϊԭ�Ϻϳ�������ﮣ�����м���Ũ����Ȼ����ˣ��õ�������1Ϊ��ʯ����Һ1�к�����������������������﮺����ᣬ����Һ1�м���̼��ƣ�̼��ƺ������ӷ�Ӧ�Ӷ�������Һ��pH��ʹ��Һ�������ӡ�������ת��Ϊ��������Һ2�к�������﮺�����ƣ�����Һ2�м���̼��ƣ��õ�̼��﮳�������Һ3������Ȼ�﮵õ�Li��Li���������ϵõ�LiH��LiH���Ȼ�����һ�������·�Ӧ����LiAlH4��
(1)������ӿ�ʯ�н�����������ʯ���������Ũ�ȡ����ȵȴ�ʩ������߷�Ӧ���ʣ�����̼����к���Һ�е��ᣬʹ������������ȫ�����������������������������Ӷ���ȥ���ʣ��ӱ�����Ϣ��������pH��СֵΪ6.5��ȷ����������ȫ������
(2)�����⣬̼��﮵��ܽ�����¶����߶���С������ˮϴ��̼��ﮣ����Լ���̼�����ʧ�����������������ƣ�����SO42-���жϳ����Ƿ�ϴ��������Ϊ��ȡ���һ��ϴ��Һ���Թ��У��μ��Ȼ�����Һ��ϡ����(������������)��
(3)�Ȼ������⻯﮷�Ӧ����������﮺��Ȼ�ﮣ�����ʽΪAlCl3+4LiH=LiAlH4+3LiCl��
(4)����ϡ�����ܽ�̼��﮵õ��Ȼ�ﮣ���Ϊ�Ȼ��ˮ�⣬Ϊ��ֹ��ˮ�⣬��Ҫ���Ȼ����������Ȼ����Һ���Ӷ��õ�LiCl���壻
(5)�������Ϣ��֪����ԭ���Ļ�ԭ����ʵָʧ��������1molLiAlH4���ṩ8mol���ӣ��൱��4molH2��LiAH4����Ч��Ϊ![]() ��0.21��
��0.21��

 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д� ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�����Ŀ����֪ij���巴Ӧ��ƽ�ⳣ���ɱ�ʾΪK=c(CH3OCH3)c(H2O)/c2(CH3OH)���÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ����400����K=32��500����K=44����ش��������⣺
��1��д��������Ӧ�Ļ�ѧ����ʽ��_________________________________ ��
��2���÷�Ӧ����H _________0��
��3����֪���ܱ������У����ijʱ�̸���ֵ�Ũ�����£�
���� | CH3OH(g�� | CH3OCH3(g�� | H2O(g�� |
Ũ��/��molL-1�� | 0.54 | 0.68 | 0.68 |
�ٴ�ʱ�¶�400�棬��ijʱ������_______���������������ͬ����
�������¶�Ϊ�����꣬�Ը��¶���ƽ��̬�״����ʵ���nΪ�����꣬��ʱ��Ӧ����ͼ���λ����ͼ��____�㣬�Ƚ�ͼ��B��D��������Ӧ������Ӧ������B_______��D��������____��

��4��һ��������Ҫ��߷�Ӧ���ת���ʣ����Բ��õĴ�ʩ��___________��
a�������¶� b��������� c��ѹ�����������
d������ˮ������Ũ�� e����ʱ���������