题目内容
【题目】为严厉打击食品生产经营中违法添加非食用物质、滥用食品添加剂,卫生部、农业部等部门联合公布了包含硫酸亚铁在内的22种“易滥用食品添加剂”名单。某同学为探究富含硫酸亚铁且保存时间较长的食品情况,设计了如下实验方案:
![]()
(1)试剂1的主要成分的化学式是________。
(2)加入新制氯水后溶液红色加深的原因是_____________(用离子方程式表示)。
(3)该同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现对褪色原因进行探究。
①提出假设
假设1:溶液中的+3价铁被氧化为更高价态的铁;
假设2:___________。
②设计方案
为了对你所提出的假设2进行验证,请写出一种实验方案:_______。
【答案】KSCN 2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3 SCN-被过量的氯水氧化 取少量褪色后的溶液,滴加过量KSCN溶液,若出现红色,则说明假设2成立,若不出现红色,则说明假设2不成立
【解析】
(1)根据实验方案,向淡黄色溶液中加入试剂1生成了淡红色溶液,说明食品中的FeSO4被空气中的O2氧化成了Fe3+,Fe3+与KSCN溶液反应生成红色的Fe(SCN)3,故答案为:KSCN;
(2)淡红色溶液中还含有较多的Fe2+,向其中加入新制氯水时,Cl2将Fe2+氧化成Fe3+,溶液中Fe3+浓度增大,生成的Fe(SCN)3浓度也增大,发生的反应有:2Fe2++Cl2===2Fe3++2Cl-、Fe3++3SCN-===Fe(SCN)3,因此溶液红色加深,故答案为:2Fe2++Cl2===2Fe3++2Cl-、Fe3++3SCN-===Fe(SCN)3;
(3)①实验中加入过量氯水,放置一段时间后,深红色褪去,说明Fe(SCN)3逐渐消失,而Fe(SCN)3的生成与Fe3+、SCN-有关,根据假设1,可能是溶液中的+3价的铁被Cl2氧化为更高价态的铁,溶液颜色褪去;分析SCN-中各元素的化合价可知,S为-2价,C为+4价,N为-3价,所以SCN-也具有还原性,故也可能是SCN-被过量的氯水氧化导致深红色褪去,故答案为:SCN-被过量的氯水氧化;
②假设Fe3+没有被氧化,而是SCN-被氧化,只要向褪色后的溶液中补充SCN-,若出现红色,说明假设2成立,反之则假设2不成立,故答案为:取少量褪色后的溶液,滴加过量KSCN溶液,若出现红色,则说明假设2成立,若不出现红色,则说明假设2不成立。

【题目】二甲醚CH3OCH3又称甲醚,熔点-141.5℃,沸点-24.9℃。由合成气(CO、H2)制备二甲醚的反应原理如下:
①CO(g)+2H2(g) ![]() CH3OH(g) △H1 =-90.0 kJ·mol-1
CH3OH(g) △H1 =-90.0 kJ·mol-1
②2CH3OH(g) ![]() CH3OCH3(g)+ H2O(g) △H2 = -20.0 kJ·mol-1
CH3OCH3(g)+ H2O(g) △H2 = -20.0 kJ·mol-1
回答下列问题:
(1)反应①在_____________(填“低温”或“高温”)下易自发进行。
(2)写出由合成气(CO、H2)直接制备CH3OCH3的热化学方程式:______________。
(3)温度为500K时,在2L的密闭容器中充入2mol CO和6molH2发生反应①、②,5min时达到平衡,平衡时CO的转化率为60%,c(CH3OCH3) = 0.2 mol·L-1,用H2表示反应①的速率是________,反应②的平衡常数K =____________。
(4)研究发现,在体积相同的容器中加入物质的量相同的CO和H2发生反应①、②,在不同温度和有无催化剂组合下经过相同反应时间测得如下实验数据:
T(K) | 催化剂 | CO转化(%) | CH3OCH3选择性(%) |
473 | 无 | 10 | 36 |
500 | 无 | 12 | 39 |
500 | Cu/ZnO | 20 | 81 |
(备注)二甲醚选择性:转化的CO中生成CH3OCH3百分比
①相同温度下,选用Cu/ZnO作催化剂,该催化剂能_______ (填标号)。
A.促进平衡正向移动 B.提高反应速率 C.降低反应的活化能
D.改变反应的焓变 E.提高CO的平衡转化率
②表中实验数据表明,在500K时,催化剂Cu/ZnO对CO转化成CH3OCH3的选择性有显著的影响,其原因是__________________________。
【题目】四氢铝锂(LiAlH4)常作有机合成的重要还原剂。以辉锂矿(主要成分Li2OAl2O34SiO2,含少量Fe2O3)为原料合成四氢铝锂的流程如图:
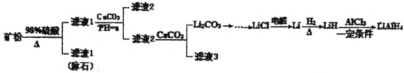
已知:①几种金属氢氧化物沉淀的pH如表所示:
物质 | Fe(OH)3 | A1(OH)3 |
开始沉淀的pH | 2.3 | 4.0 |
完全沉淀的pH | 3.7 | 6.5 |
②常温下,Ksp(Li2CO3)=2.0×10-3。Li2CO3在水中溶解度随着温度升高而减小。
回答下列问题:
(1)上述流程中,提高“酸浸”速率的措施有____ (写两条);加入CaCO3的作用是____,“a”的最小值为____。
(2)用热水洗涤Li2CO3固体,而不用冷水洗涤,其目的是___;检验碳酸锂是否洗净的实验操作是___。
(3)写出LiH和AlCl3反应的化学方程式:___(条件不作要求)
(4)设计简单方案由Li2CO3制备无水LiCl:___。
(5)在有机合成中,还原剂的还原能力通常用“有效氢”表示,其含义是1克还原剂相当于多少克氢气的还原能力,LiAlH4的“有效氢"为___。(结果保留2位小数)